
导读
肺癌是全球癌症相关死亡的主要原因之一,占癌症相关死亡率的18%,占癌症发病率的11% 。其中非小细胞肺癌(NSCLC)是其最常见的肺癌类型,约占所有病例的85%。肺癌具有高度异质性,研究人员可以通过多部位、多时间点的测序观察肿瘤内异质性(Intratumour heterogeneity, ITH),进而推断肿瘤的系统发育。但此前的研究多是利用原发肿瘤样本的多区域测序,并且对于给定的肿瘤类型,仅限于数量较少的患者,这大大限制了基因组和临床分析的统计能力。因此,人们对于肺癌异质性背后生物学机制的了解并不全面。
TRACERx是一项前瞻性NSCLC多中心癌症研究项目(NCT01888601),旨在描述肿瘤从诊断、手术切除到治愈或疾病复发的整个演变过程,提供全面的NSCLC疾病描述,包括肿瘤多个区域的详细临床注释和广泛的基因组表征、以及临床结局。TRACERx的共同主要终点是确定ITH与临床结局之间的关系,以及复发疾病中辅助化疗对ITH的影响。
近日,TRACERx联盟的成员团队在国际顶尖期刊Nature发表了系列文章,报告了基于TRACERx试验中临床肺癌样本的分析结果。其中,题为“The evolution of lung cancer and impact of subclonal selection in TRACERx”的文章,通过分析来自TRACERx项目421例NSCLC患者手术或随访中采集的1644个肿瘤区域数据,破译肺癌的演变,并确定ITH和临床结果之间的关系。研究人员定义了驱动因素、突变过程和全基因组加倍(WGD) 事件之间的进化依赖关系,同时证明了克隆扩增、WGD和拷贝数不稳定性在确定NSCLC复发时间和模式中的重要性,并提供了全面的临床NSCLC进化数据资源。
主要研究内容
该研究涉及的TRACERx队列是英国19家医院前瞻性招募的首批421名NSCLC患者,根据种族、年龄、性别和吸烟状况进行划分,代表了早期未经治疗的NSCLC人群。该队列包括233名男性和188名女性,中位年龄为69岁,210名患者为I期NSCLC,132名患者为II期NSCLC,79名患者为III期NSCLC。在初次手术或随访中,共有1644个肿瘤区域的样本进行了全外显子组测序(WES)及后续分析。

图1. TRACERx队列特征分析,来源:Nature
研究队列中43%的NSCLC患者是吸烟者,50%患者是在诊断前1年以上停止吸烟的前吸烟者,7%的患者是一生中吸烟少于100支的从不吸烟者。研究人员探索了烟草、烟雾对NSCLC进化的影响,并评估了确定观察吸烟介导突变可能性的临床特征。突变特征的提取和分析揭示了与烟草烟雾有关的两个突变过程:SBS4和SBS92。这与前期的研究结果一致,即在肺腺癌(Lung Adenocarcinoma, LUAD)中,随着烟草烟雾暴露以包/年为单位测量,SBS4相关的截尾突变的百分比显著增加;相比之下,在肺鳞状细胞癌 (Lung squamous cell carcinoma, LUSC)中,与烟草烟雾接触相关的SBS92的截断突变比例显著增加。因此,以上数据表明,SBS4相关突变和SBS92相关突变可以分别作为LUAD和LUSC中吸烟介导突变量的替代标记。通过WES分析,215例长期吸烟的LUAD患者中有161例显示出明显的吸烟介导诱变特征。吸烟介导的突变SBS4或SBS92的高置信度检测,仅发生在吸烟少于15年的LUAD患者的少数肿瘤中。考虑到TRACERx研究中大多数LUAD患者在14-18岁开始吸烟,这些数据表明,在30-35岁之前戒烟可能会降低吸烟相关肺癌的风险,这与已有的流行病学分析一致。在LUAD中,与左侧相比,右侧肺肿瘤的SBS4相关突变数量显著增加;与下肺叶相比,上肺叶或中肺叶的SBS4相关突变数量显著增加。这些数据支持了一种假设,即不同肺叶间气道长度、通气和灌注的差异可能导致烟草致癌物质暴露的变化,并支持了肺部不同解剖部位肿瘤起始率的既定差异。此外,部分重度吸烟史的NSCLC患者肿瘤具有与从未吸烟者肿瘤相似的EGFR突变检出率,以及RET、ROS1、ALK和MET致癌基因的同源异构体检出率,表明这些患者具有相似的病因和发病机制。
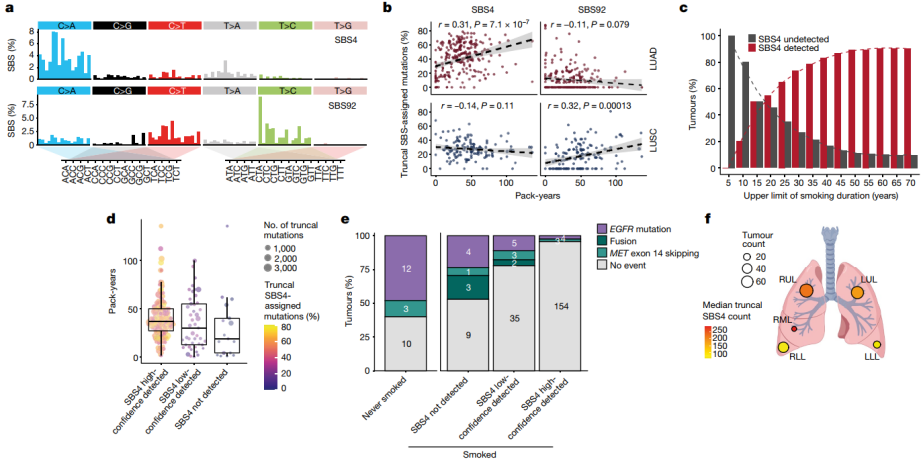
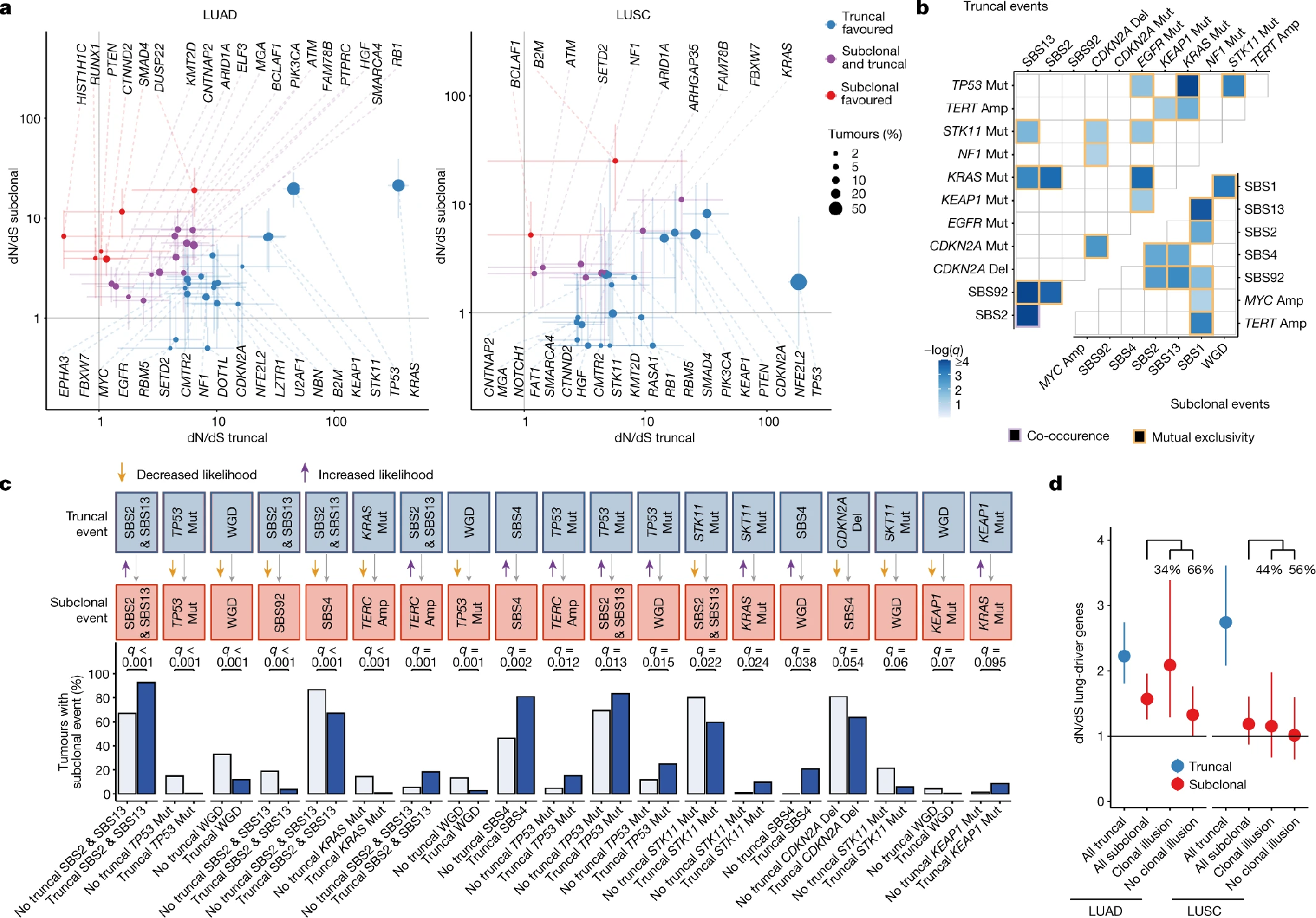
图2. NSCLC中SBS4相关突变的临床和生理决定因素,来源:Nature研究团队使用dNdScv方法直接量化了常见NSCLC基因突变的躯干(truncal)和亚克隆选择。在大多数癌症基因(LUAD和LUSC中分别有68%和84%的常见癌症基因)中,躯干突变的选择信号强于亚克隆突变。在许多通常被认为是肿瘤起始事件的癌症基因突变中存在显著的亚克隆选择,包括LUAD中的STK11、TP53和KRAS。在LUAD中,大多数频繁突变的癌症基因(40个中有22个)受到显著的阳性亚克隆选择,包括PIK3CA, RB1和SMARCA。在这22个基因中的7个,包括HIST1H1C、KMT2D、PTEN、RUNX1和SMAD4,在躯干突变中没有检测到显著的阳性选择。这一结果表明,这些突变在NSCLC晚期而不是早期进化中起作用。在LUSC中,31个频繁突变的癌症基因中,有11个存在显著的亚克隆选择,包括ATM、B2M、KEAP1、NFE2L2、PIK3CA和SETD2。
图3. NSCLC中SBS4相关突变的临床和生理决定因素,来源:Nature
TRACERx研究的一个主要终点是探索基因组ITH与临床结果之间的关系。研究发现,体细胞拷贝数改变(SCNA)的ITH与较短无病生存期(DFS)之间存在显著关联,突变ITH与DFS之间无显著关系。鉴于前期研究表明WGD与预后不良、癌症基因组进化加速和ITH有关,研究团队分析了WGD事件的异质性是否与预后相关。结果发现,虽然任何WGD事件的存在均与预后无关,但亚克隆性WGD事件的存在与较短的DFS显著相关。在包括SCNA ITH在内的多变量模型中,亚克隆WGD是DFS的独立预测因子。亚克隆扩增较大NSCLC患者的DFS显著缩短。这些数据强调,在探索基因组ITH与预后之间的关系时,不仅要考虑亚克隆突变的数量或比例,还需要考虑每个肿瘤区域特定的克隆结构。最后,研究人员将已有的SCNA ITH和两个新的基于ITH的预后指标(亚克隆WGD和近期的亚克隆扩增)结合在一个包括肿瘤分期、年龄、组织学和辅助治疗状态的多变量模型中。结果显示,近期亚克隆扩增评分仍是DFS的重要预测因子。这一结果证明近期克隆扩增超出了标准临床指标的预后价值。总的来说,这些数据表明,几种进化指标可以一起用于预测未来复发的可能性、时间和部位。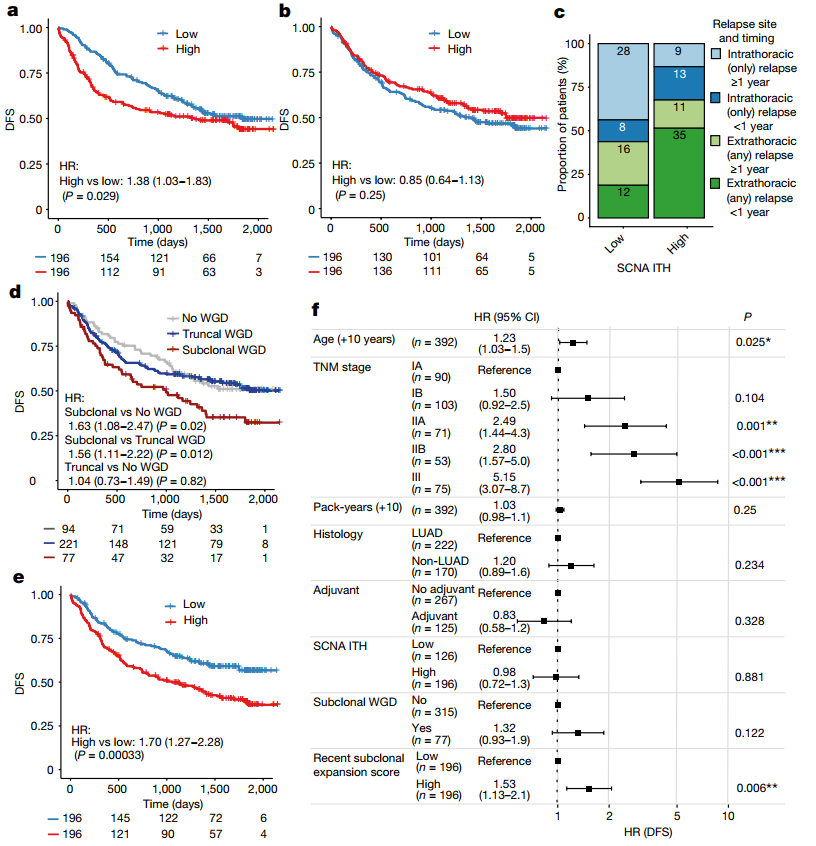
图4. TRACERx队列中ITH与预后的关系,来源:Nature综上所述,研究团队通过分析400多个拥有多区域测序的NSCLC患者,能够在基因水平上量化未经治疗早期NSCLC的亚克隆突变选择。研究发现,在至少一个肿瘤区域有近期亚克隆扩增证据的肿瘤患者的DFS较短,这表明持续的克隆扩增可能导致更糟糕的结果,例如癌症转移扩散的可能性增加。该研究提供了一个广泛采样的肿瘤数据集,包括临床和基因组学数据,有助于促进未来的癌症进化研究,进一步了解肿瘤生物学,以改善癌症患者预后。TRACERx是首个关于肺癌如何发展的长期研究。TRACERx的首席临床医生、伦敦大学学院Francis Crick研究所Charles Swanton教授表示:“TRACERx认识到癌症不是一成一变的,我们治疗患者的方式不应该是一样的。TRACERx项目的特别强大之处是,它以动态、系统的眼光看待肿瘤治疗。通过观察整个肿瘤,我们可以观察到这些细胞群是如何相互作用的,甚至是如何与另一个细胞群竞争的,这有助于我们获得有价值的信息,了解肿瘤复发的方式以及它可能发生的时间。我们还可以观察到肿瘤随着时间的推移、扩散和对治疗的反应,为未来数百万患者提供了希望。”研究人员还指出,虽然这项研究是在肺癌患者身上进行的,但相关发现也可以应用于其他类型的癌症,如皮肤癌或肾癌。1.Frankell, A.M., Dietzen, M., Al Bakir, M. et al. The evolution of lung cancer and impact of subclonal selection in TRACERx. Nature (2023).https://www.nature.com/articles/s41586-023-05783-5
2.Genetic clues reveal lung cancer's next move
https://medicalxpress.com/news/2023-04-genetic-clues-reveal-lung-cancer.html
[以上文章来源于测序中国 ,作者小鹿-先森]




 技术咨询:
技术咨询: