多组学整合发Nature Genetics!同济团队基因组+转录组+蛋白组+代谢组+空间组学,揭示肾癌全新高危亚型
2026-04-27
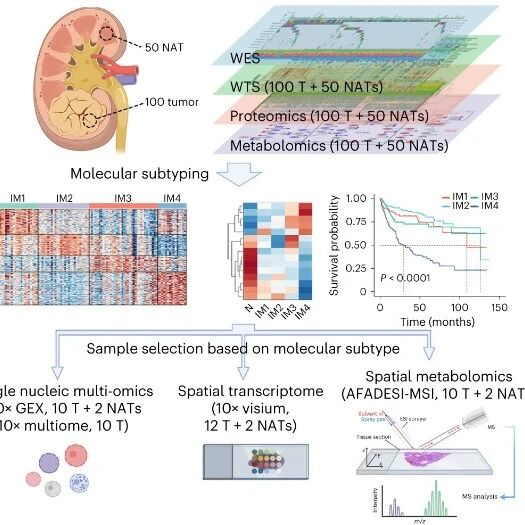
文献标题:Multi-omic profiling of clear cell renal cell carcinoma identifies metabolic reprogramming associated with disease progression 文献来源:同济大学附属同济医院 发表期刊:Nature Genetics(IF=25.2,JCR Q1区,中科院1区) 发表时间:2024年2月 研 究 背 景 肾细胞癌是全球十大最常见的恶性肿瘤之一,其中透明细胞肾细胞癌(ccRCC)占比超过70%,是肾癌最常见的类型。 这种癌症具有较高的死亡率、侵袭性和转移率,约30%的患者在首次确诊时就已经出现转移! 代谢失调一直是ccRCC的关键特征,但以往的研究大多只关注单一组学层面,基因组、表观基因组与代谢紊乱之间的关系在很大程度上未被探索。 多组学分析:技术路线全解析 这项研究的核心亮点在于其全面而深入的多组学分析策略。研究团队对同济医院RCC队列的100例ccRCC患者进行了系统性的多维度分析。 图1.TJ-RCC队列的多组学表征 基因组层面:全外显子测序(WES) 研究首先通过全外显子测序技术,对肿瘤样本进行全面的基因突变分析。结果显示,最常见的突变基因与之前的研究结果一致,为后续分析提供了可靠的基因组基础。 技术细节 测序深度:肿瘤组织平均测序深度为150×,正常组织为50× 突变检测:使用GATK标准流程识别单核苷酸变异(SNV)和小片段插入缺失(Indel) 驱动基因分析:重点关注VHL、PBRM1、SETD2、BAP1等已知的ccRCC驱动基因 关键发现 1.VHL基因突变率为85%,与之前研究一致 2.发现了一些罕见的基因融合事件,可能与肿瘤异质性相关 3.突变特征分析显示,APOBEC酶相关的突变特征在部分肿瘤中显著 转录组层面:全转录组测序(WTS) 通过全转录组测序,研究人员获得了基因表达的全景图谱。主成分分析显示,肿瘤组织和邻近正常组织之间存在显著区别,证实了转录水平的明显差异。 分析方法 差异表达分析:比较肿瘤与正常组织的基因表达差异 通路富集分析:使用GSEA方法识别显著富集的生物学通路 免疫细胞浸润评估:通过CIBERSORTx算法估算肿瘤微环境中各种免疫细胞的比例 技术亮点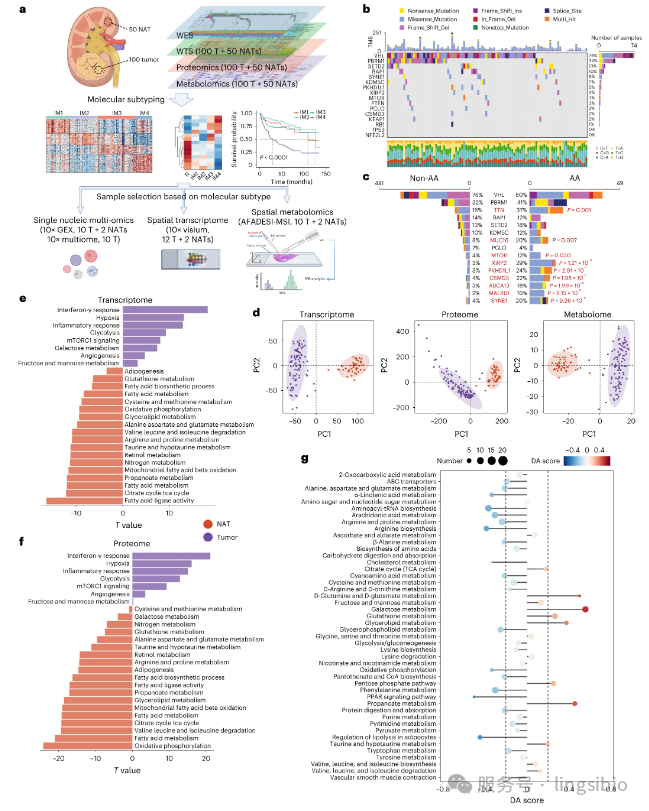

研究人员开发了定制化的生物信息学流程,专门针对ccRCC的转录特征进行优化。例如,他们建立了ccRCC特异的基因集,用于更准确地评估代谢相关通路的活性。
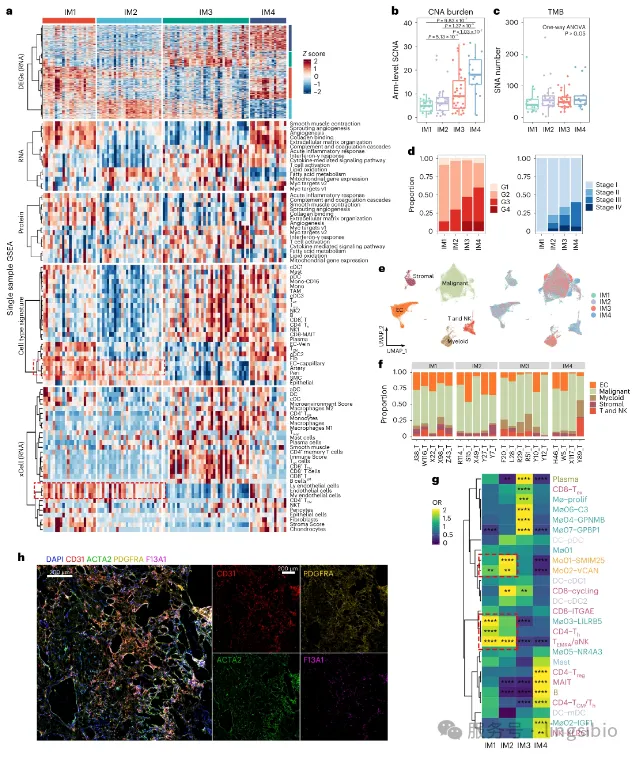
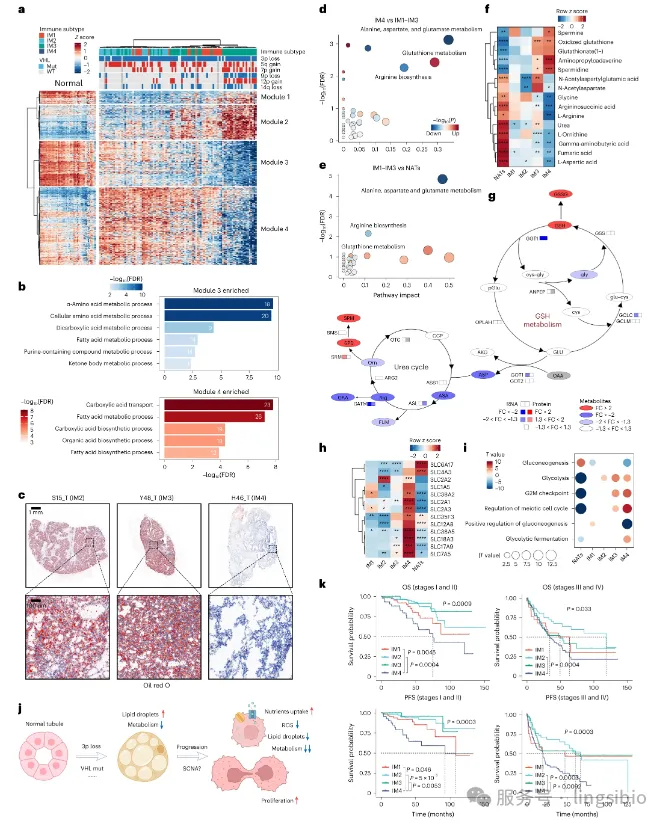
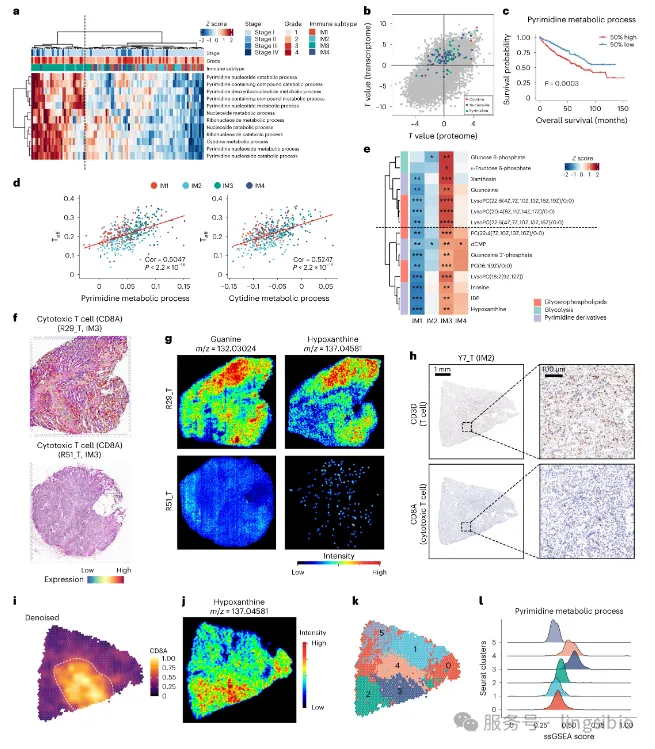
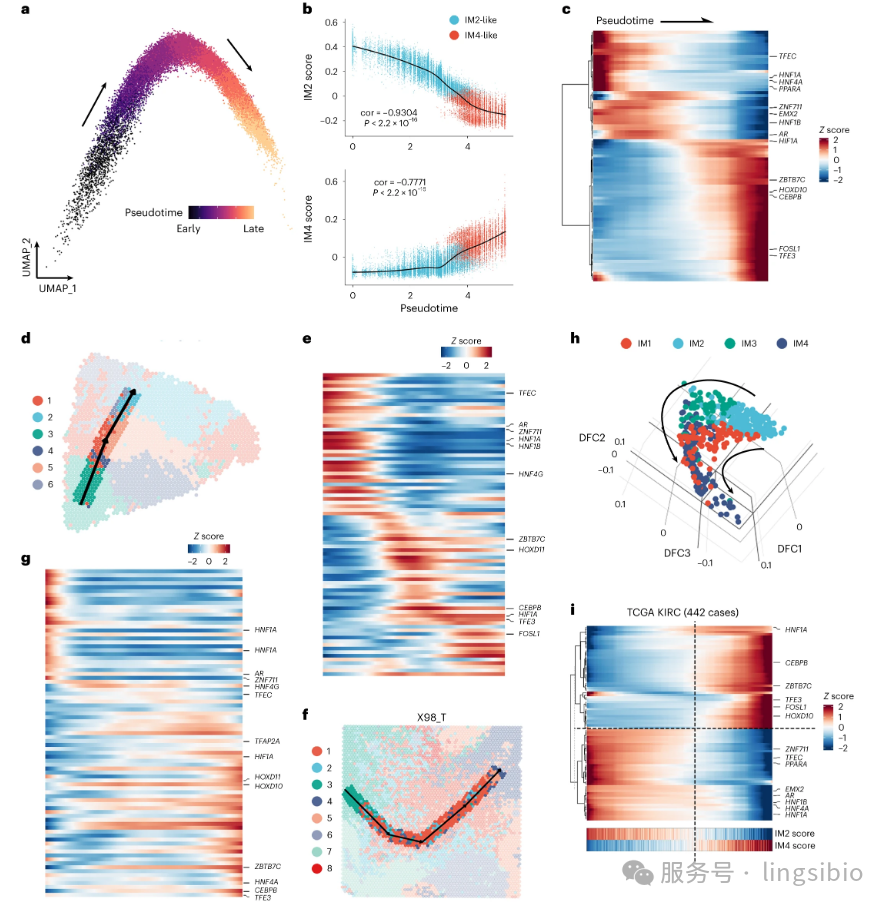
蛋白质组层面:定量蛋白质组学 蛋白质是基因功能的执行者。研究团队采用先进的质谱技术,对样本中的蛋白质进行定量分析,揭示了基因表达与蛋白质水平之间的复杂关系。 实验流程 蛋白质提取与酶解:使用FASP方法提取蛋白质,胰蛋白酶消化成肽段 TMT标记:使用11-plex TMT试剂对肽段进行同位素标记 LC-MS/MS分析:使用Orbitrap Fusion Lumos质谱仪进行数据采集 数据分析:使用MaxQuant软件进行蛋白质鉴定和定量 整合分析策略 研究人员特别关注了转录组与蛋白质组数据的一致性。他们发现: 1.约60%的基因在mRNA和蛋白质水平上表达趋势一致 2.40%的基因存在转录后调控,mRNA与蛋白质水平不相关 3.代谢相关基因更倾向于在蛋白质水平上表现出显著变化 代谢组层面:非靶向代谢组学 代谢组学分析采用了液相色谱-质谱联用(LC-MS)和气相色谱-质谱联用(GC-MS) 两种技术平台,全面检测了样本中的小分子代谢物。 LC-MS非靶向代谢组学 覆盖范围:主要检测极性代谢物,如氨基酸、有机酸、核苷酸等 色谱条件:HILIC色谱柱,正负离子模式切换 数据采集:全扫描与数据依赖采集(DDA)模式结合 GC-MS非靶向代谢组学 覆盖范围:主要检测挥发性代谢物和衍生化后的代谢物,如脂肪酸、糖类等 衍生化方法:使用MSTFA进行硅烷化衍生 数据分析:使用AMDIS软件进行峰解卷积和代谢物鉴定 通过这种双重验证策略,研究团队共鉴定了500多种代谢物,构建了ccRCC最全面的代谢图谱之一。 单细胞层面:单细胞多组学测序 为了深入解析肿瘤微环境的异质性,研究团队对20个ccRCC样本进行了单细胞核转录组测序(snRNA-seq),并对其中10个样本进行了单细胞ATAC多组学测序(包括snRNA-seq和snATAC-seq)。 技术挑战与解决方案 挑战:肾癌组织富含脂滴,传统单细胞分离方法效率低 解决方案:采用核分离策略,避免脂滴干扰 细胞数:平均每个样本获得约8,000个高质量单细胞数据 细胞类型鉴定 通过聚类分析和已知标记基因,研究人员鉴定了10种主要的细胞类型: 1.肿瘤上皮细胞(多个亚群) 2.T细胞(CD4+、CD8+、调节性T细胞) 3.髓系细胞(巨噬细胞、树突状细胞) 4.内皮细胞 5.成纤维细胞 6.正常肾小管上皮细胞 关键发现 在IM4(DCCD)亚型中,肿瘤细胞表现出独特的转录状态: 1.脂质代谢相关基因显著下调 2.而糖酵解和氨基酸转运相关基因上调 3.这种代谢重编程可能是其侵袭性表型的基础 空间层面:空间转录组与代谢组学 研究还进行了空间转录组学和空间代谢组学分析。 通过对12个肿瘤切片和2个正常对照样本的分析,研究人员能够在组织原位同时获取基因表达和代谢物分布信息。 空间转录组学 技术原理:将组织切片放置在带有空间条形码的芯片上 分辨率:每个斑点直径55μm,包含约10个细胞 数据分析:使用Seurat和SPOTlight进行细胞类型解卷积 空间代谢组学 研究团队开发了一种基于质谱成像(MSI)的空间代谢组学方法: 样本制备:组织切片厚度10μm,进行基质辅助激光解吸电离(MALDI)前处理 数据采集:使用timsTOF fleX质谱仪,空间分辨率20μm 代谢物鉴定:与LC-MS/MS数据关联,提高鉴定准确性 空间分析发现 代谢物分布异质性:不同肿瘤区域的代谢物组成差异显著 免疫细胞-代谢物共定位:在T细胞富集区域,嘧啶代谢物水平较高 肿瘤边界特征:侵袭前沿的肿瘤细胞表现出独特的代谢特征 四大发现:重新定义肾癌分型 通过这一系列精密的多组学分析,研究团队取得了四项突破性发现: 发现一:四种免疫亚型 研究将ccRCC样本分为4种免疫亚型:IM1(血管丰富型)、IM2(高代谢型)、IM3(T细胞浸润型)和IM4(TAM富集,去脂质透明化型)。 生存分析显示: IM2亚型患者的总生存期和无进展生存期最好,而IM4肿瘤与较差的预后相关。 图2.基于TME的ccRCC分子亚型分析 发现二:独特的DCCD亚型 研究确定了一个独特的亚型——去透明细胞分化(DCCD)-ccRCC(对应IM4亚型)。 这种亚型的癌细胞具有脂滴少、代谢活性降低、营养吸收能力强、增殖率高的特点,预后极差。 图3.DCCD亚型在ccRCC中表现出剧烈代谢障碍和更差结果 发现三:空间异质性证据 空间组学分析揭示了ccRCC的肿瘤内异质性(ITH)。 在IM3亚型的样本中,研究人员发现嘧啶衍生物与肿瘤浸润淋巴细胞(TILs)之间存在潜在相关性。 图4.TME中免疫与代谢异质性的相关性 发现四:代谢重编程模式 IM4肿瘤表现出独特的代谢特征,脂肪酸和氨基酸代谢通路明显下调。 通过单细胞和空间轨迹分析,研究证明DCCD是ccRCC进展的一种常见模式。 图5.利用多组学数据确定DCCD轨迹 临床意义:从分型到精准治疗 这项研究的最大价值在于其直接的临床转化潜力。 研究发现,即使在I期患者中,DCCD也与较差的预后和较高的复发率相关,这表明仅通过肾切除术无法治愈这类患者。 基于这一发现,研究团队提出了一种基于亚型特异性免疫细胞浸润的治疗策略。 对于不同亚型的患者,可以采取差异化的治疗方案: IM1和IM2亚型:可能对传统的靶向治疗反应良好 IM3亚型:免疫治疗可能更为有效 IM4(DCCD)亚型:需要开发针对其独特代谢特征的新型疗法 技术突破:多组学整合的典范 这项研究代表了多组学技术在癌症研究中的成功应用典范。 通过整合基因组、转录组、蛋白质组、代谢组和空间组学数据,研究团队构建了ccRCC的全方位分子图谱。 特别值得关注的是空间代谢组学技术的应用。 这项技术能够在保留组织空间结构的同时,分析代谢物的分布情况,为理解肿瘤微环境中代谢物与细胞类型的相互作用提供了前所未有的视角。 研究还展示了单细胞多组学技术的强大能力。 通过同时分析基因表达和染色质可及性,研究人员能够更深入地理解ccRCC中不同细胞类型的表观遗传调控机制。 这项研究的意义不仅在于发现了ccRCC的新亚型,更在于建立了一套完整的分子分型诊疗体系。 研究团队已经将这一体系应用于临床实践,为难治性肾细胞癌患者提供了新的治疗机会。随着多组学技术的不断发展和成本的降低,类似的精准医疗模式有望推广到更多癌症类型。 未来,每位癌症患者都可能获得基于多组学分析的个性化治疗方案,真正实现"一人一策"的精准医疗愿景。 E N D![]()








 技术咨询:
技术咨询: