Bulk-RNAseq联合scRNA-seq揭示胰腺癌类器官中肿瘤相关巨噬细胞多样性与其促癌细胞相关性
2024-12-10

本期介绍的这篇文章是来自东京大学医学研究所再生医学学部的Hideki Taniguchi研究团队在Biomaterials上发表的,题为A pancreatic cancer organoid incorporating macrophages reveals the correlation between the diversity of tumor-associated macrophages and cancer cell survival的研究性论文。(https://pubmed.ncbi.nlm.nih.gov/39348736/)
摘要:
胰腺导管腺癌(PDAC)是一种预后不良的进行性癌症。它包含一个复杂的肿瘤微环境(TME),包括各种基质细胞类型,与其恶性程度高度相关。由于缺乏人类PDAC-TME的研究模型,此前人们对TME内的细胞通信较难了解。类器官技术的发展使得人们可以通过结合基质细胞和重构ECM网络来实现体外重建TME。
本文研究团队通过将患者来源的癌细胞与人诱导多能干细胞(hiPSC)来源的间充质细胞和内皮细胞共培养,在体外建立了PDAC的类器官,即融合胰腺癌类器官(FPCO)。他们还将来自THP-1细胞系的巨噬细胞M0-FPCO纳入其中,通过联合分析Bulk RNA-seq和单细胞RNA-seq,他们发现M0-FPCO (FPCO-Mac)中的巨噬细胞失去了促炎症的特征,获得了促血管生成的特征。而内皮细胞网络的形成增强。M0-FPCO中含有5个与人PDAC组织中相应TAM相似的TAM亚群,包括SPP1+-TAM,与肿瘤血管生成和细胞增殖相关。PDAC细胞可以在TAM存在的类器官中存活更长时间。与PDAC细胞增殖和存活时间延长一致,PDAC亚群具有增殖特征,如M0-FPCO增加。因此,通过纳入巨噬细胞建立的PDAC类器官,不仅可以概括TAM的多样性,也能明确TAM在内皮网络形成和PDAC细胞特性调节中的作用。
结果:
1.建立包括巨噬细胞在内的PDAC类器官
为了确认髓系细胞的丰度,研究者们使用髓系细胞标志物CD11b的抗体,通过免疫荧光(IF)分析PDAC患者组织。
随即发现PDAC患者胰腺肿瘤区域的CD11b+细胞较之邻近正常区域明显富集(图1A和B)。基于这一发现,他们首次将巨噬细胞纳入PDAC类器官中,作为TME的主要组成部分。
他们使用THP-1细胞进行类器官培养,并用慢病毒kusabira-orange (KuO)追踪标记THP-1细胞,分选KuO阳性THP-1细胞(图1C)。为了生成含有巨噬细胞的类器官,他们利用THP-1细胞衍生的M0-Mac与PDAC细胞(用荧光素酶和GFP标记)、hipsc衍生的间充质细胞和内皮细胞(hiPSC-MCs和hiPSC-ECs)在超低附着板上共培养24小时,形成多细胞球体。随后,将其转入气液界面培养并维持6天(图1D)。KuO标记的巨噬细胞分布在FPCO内,如均匀的KuO信号所示(图1E右侧)。H&E染色显示,FPCO和M0-FPCO均能有效复制间质致密的PDAC的导管结构(图1F)。补充材料S1也证明了这种可重复性。

为了分析类器官内巨噬细胞的细胞特性,他们从M0-FPCO中分离出KuO-Mac(图2)、RT-qPCR分析检测M1和M2标记物。结果显示,与细胞因子诱导的M1- Mac相比,M0-FPCO (FPCO-Mac)中的巨噬细胞表达CD80、CXCL10和TNFA等经典M1标记物,与M0-Mac相比,表达CD163、MRC1/CD206、IL10和CCL17等经典M2标记物(补充材料S2A)。但是,FPCO-Mac没有表现出细胞因子诱导的M2-Mac的典型基因表达模式。于是他们假设FPCO-Mac具有不同于M1或M2 mac的独特细胞群。
2.巨噬细胞在FPCO中的功能分析

通过Bulk-RNAseq,研究者们将FPCO-Mac的基因表达谱与细胞因子诱导的M1-Mac、M2- mac、M0-Mac和THP-1细胞的基因表达谱进行了比较(图1G)。由Bulk-RNAseq数据生成的主成分分析图表明,FPCO-Mac获得了明显特征(图1H)。因为FPCO-Mac表达的TAM标记物在M0-Mac和M0-Mac中均未表达,因此,他们认为FPCO-Mac的独特特征是由FPCO-TME诱导的。
通过IF分析共培养7天的M0-FPCO,并将其与人PDAC组织进行比较,结果表明,在M0-FPCO中,CD11b+CD163+细胞比CD11b+CD80+细胞更丰富,这与人PDAC组织相似(图2A和B),这表明CD163的大量表达可能是TAM的明确标志物。
基因集富集分析(GSEA)显示FPCO-Mac上调血管生成和缺氧过程,而炎症过程(如INF-γ反应)则下调。比较FPCO-Mac和M0-Mac之间的差异表达基因(DEGs),发现FPCO-Mac中血管发育基因和缺氧反应上调,而免疫反应相关基因下调(图2C)。除了转录组分析外,细胞因子阵列分析显示,几丁质酶-3样蛋白1 (CHI3L1)和骨桥蛋白(OPN)以及基质金属蛋白酶9 (MMP9)在M0-FPCO中增加(图2D),这与血管生成有关。表皮生长因子(EGF)在FPCO组的释放量高于M0-FPCO组。
IF检测M0-FPCO的血管结构显示,与FPCO相比,M0-FPCO中CD31阳性细胞更丰富且相互连接(图2E和F);然而,M0-FPCO内部的微血管结构无法维持管状结构的通畅(图2G)。因此,FPCO- mac可以刺激M0- FPCO的血管生成;但并没有完全建立内皮细胞的完整性。
3.FPCO巨噬细胞促进癌细胞存活
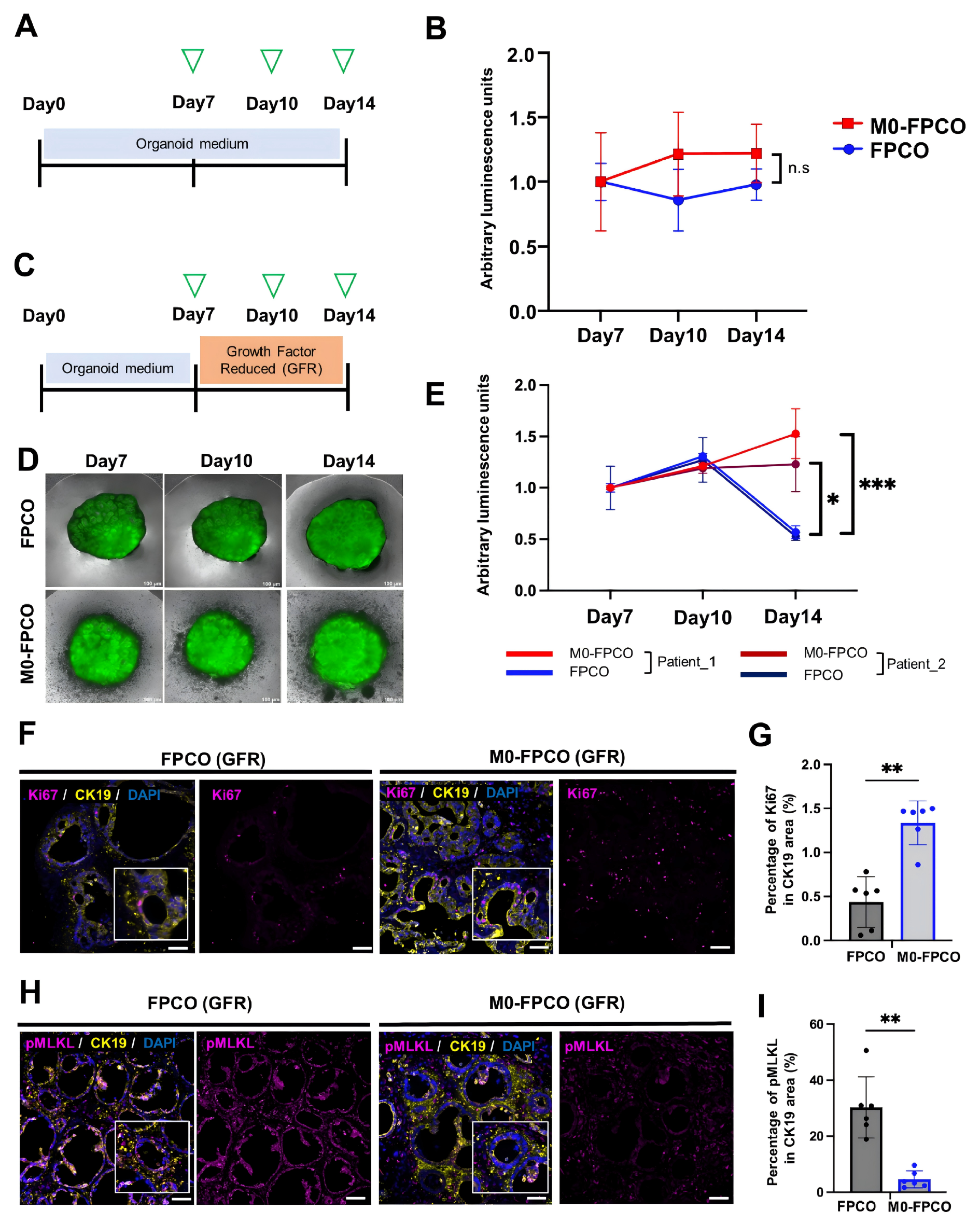
接下来,他们研究了TAMs影响癌细胞特征或维持癌症干细胞的可能性。观察到,在延长培养期间,与FPCO相比,M0-FPCO中的PDAC细胞数量略有增加(图3A和B)。
考虑到两个可能影响类器官内PDAC细胞增殖能力的潜在原因可能是PDAC细胞对培养基中提供的细胞因子的增强反应或是TAMs中存在细胞相互作用赋予PDAC细胞促增殖或抗细胞死亡特性。
于是他们在没有EGF和FBS(生长因子降低,GFR)的情况下维持FPCO和M0-FPCO培养 1周(图3C)。在没有外源性细胞因子的情况下(第7-14天),FPCO和M0-FPCO的宏观外观相似(图3D);然而,定量分析显示,FPCO中的癌细胞数量在第10至14天之间减少,而在M0-FPCO中癌细胞数量保持不变(图3E)。来自不同患者的其他PDAC细胞之间也是一致现象,这表明PDAC细胞在M0-FPCO培养中维持的稳定性。
IF分析显示,与FPCO相比,M0-FPCO中存在更多的Ki67+DAPI+ CK19+细胞(图3F和G)。此外,由于PDAC细胞稀疏地位于FPCO中间,因此他们也检查了细胞凋亡。发现与M0-FPCO相比,FPCO中pMLKL阳性的PDAC细胞有所增加(图3H和I)。综合来看,这些结果表明FPCO- mac不仅促进PDAC细胞的增殖,而且有助于PDAC细胞的存活。
4.GFR-M0-FPCO中PDAC细胞表达与PDAC细胞存活相关的因子
为了深入了解M0-FPCO长期维持的机制,研究者们通过Bulk-RNAseq对GFR-M0-FPCO中的PDAC细胞进行分析。比较第14天FPCO中的PDAC细胞和M0-FPCO中的PDAC细胞,发现与FPCO相比,M0-FPCO分离的PDAC细胞数量更多(图3E)。补充图也展示了M0-FPCO中细胞周期相关特征的增加。
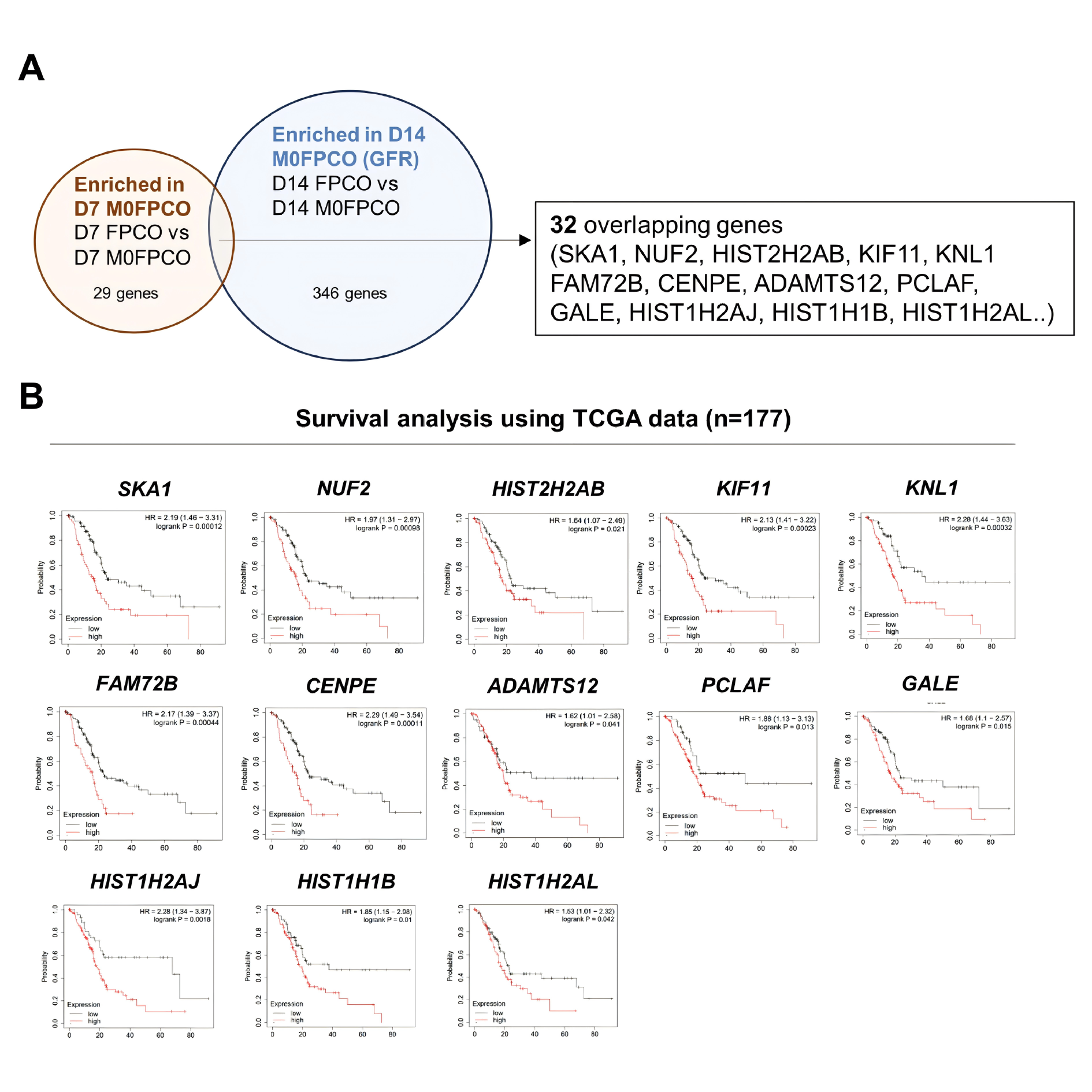
因此,他们比较M0- FPCO与FPCO中PDAC细胞在第7天和第14天的基因表达谱,选择了32个在TAMs存在下上调的基因,如图4A所示。其中,有几个基因与癌细胞增殖和抑制癌细胞死亡相关。基于TCGA数据集,他们发现这32个基因中有13个基因与PDAC患者的低生存率相关(图4B)。这些结果为M0-FPCO长期维持PDAC细胞的增殖和存活能力的机制提供了新思路。
5.M0-FPCO获得肿瘤相关巨噬细胞的多样性
接下来他们使用单细胞RNAseq (scRNA-seq)对第14天的M0-FPCO进行分析,选择TAMs作为CD11b+细胞,并进行聚类分析,发现了来自M0-Mac的五个不同的TAMs亚群,包括SPP1、C1QC、TREM2、增殖、上皮样TAMs(图5A和B)。这些在PDAC患者组织也曾被报道。
根据scRNA-seq的数据,他们检测了TAMs是否特异性表达OPN、 CHI3L1和MMP9,在细胞因子阵列分析中,与FPCO相比,M0-FPCO中这些基因表达上调(图2D)。因此,在M0-FPCO中,巨噬细胞特异性分泌OPN、CHI3L1和MMP,而在巨噬细胞存在时,间充质细胞中可能会轻微上调FN1和COL1A1。
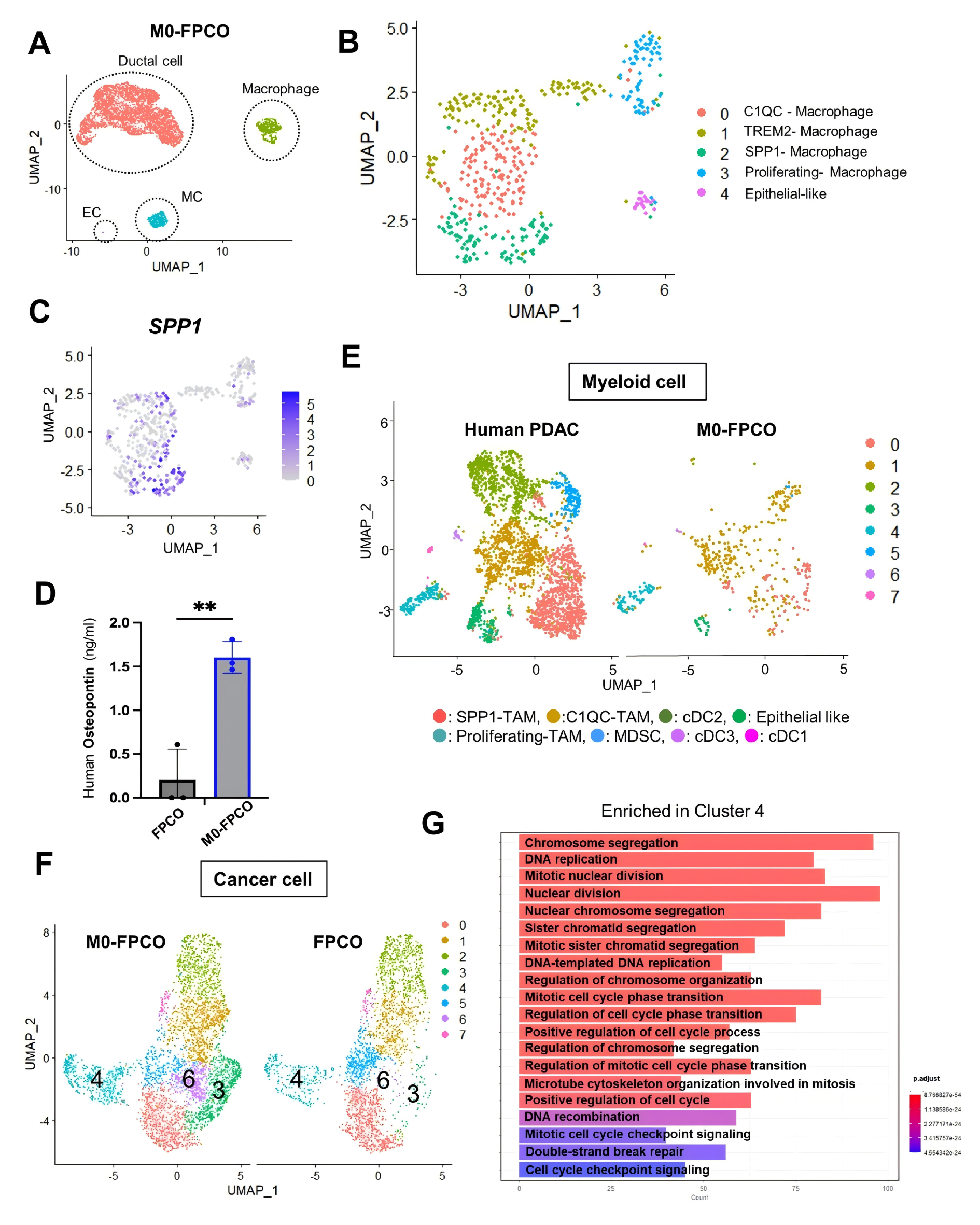
与细胞因子阵列数据(图2D)一致,M0-FPCO中SPP1的翻译产物OPN的分泌量更高,这进一步支持了SPP1- TAM是在M0-FPCO中出现的观点(图5D)。此外,利用人PDAC数据和M0-FPCO对骨髓细胞进行综合分析,结果显示PDAC-TAM和M0-FPCO均分为8个簇(图5E,图5E)。而且PDAC还含有树突状细胞和骨髓抑制细胞群,而这些在M0-FPCO中不存在。这些发现证实,该类器官模型可以准确概括人类PDAC组织中TAMs的多样性。
讨论:
本文所构建的PDAC类器官,首次概括了TAMs的多样性,并通过Bulk-RNAseq联合scRNA-se揭示了每个TAMs功能及其对应的特定的亚群。这些发现可以为抗癌药物研发提供方向,为设计针对TAMs的药物筛选时作为有用工具。
 技术咨询:
技术咨询: