scRNASeq联合Bulk RNASeq揭示内皮细胞Pim3激酶在肺转移过程中保护血管屏障的机制
2024-12-10
本期介绍的是来自赫尔辛基大学的Olli Carpen和 Pipsa Saharinen教授团队于2024年12月3日发表在Nature Communications上的文章。https://doi.org/10.1038/s41467-024-54445-1。
摘要:
内皮细胞(ECs)可以形成组织特异性屏障,助于癌细胞远处转移。然而,转移性生态位中ECs的分子调控机制尚不清楚。在这篇研究中,研究者们使用单细胞RNA测序(scRNASeq)分析了黑色素瘤细胞到达肺转移生态位6小时后ECs的转录重编程。他们发现了一个反应性毛细血管EC簇(rCap),rCap富集血管生成和炎症途径,在人肺数据集中也存在。而JAK-STAT激活的致癌Pim3激酶是rCap的标志物,同样在自发性转移模型中上调。而他们发现抑制PIM可增加血管渗漏和转移性,且能降低连接蛋白cadherin-5和连环蛋白α, β和δ从而损害EC屏障。这些结果表明了肺内皮的可塑性及其对PIM3的保护作用,这可能会削弱PIM抑制剂在癌症治疗中的效果。
结果:
1.反应性毛细血管内皮细胞在转移性肺中富集
为了研究EC屏障在肺转移定殖过程中的调节作用,他们使用高侵袭性小鼠黑色素瘤模型B16-F10在同基因C57BL/6小鼠中诱导转移,尾静脉注射黑色素瘤细胞到小鼠体内,并观察肺部定植。他们发现注射几分钟后,在循环和肺毛细血管内检测黑色素瘤细胞,呈细胞簇状。6 h后肺内可见较小的黑色素瘤细胞簇和单个细胞,12 h后数量急剧下降。从第3天开始结节数量也逐渐增加。与门静脉注射诱导肝转移相比,尾静脉注射B16-F10后,肝转移的发生速度明显减慢,到第9天,肝脏表面仅出现少量小转移结节。
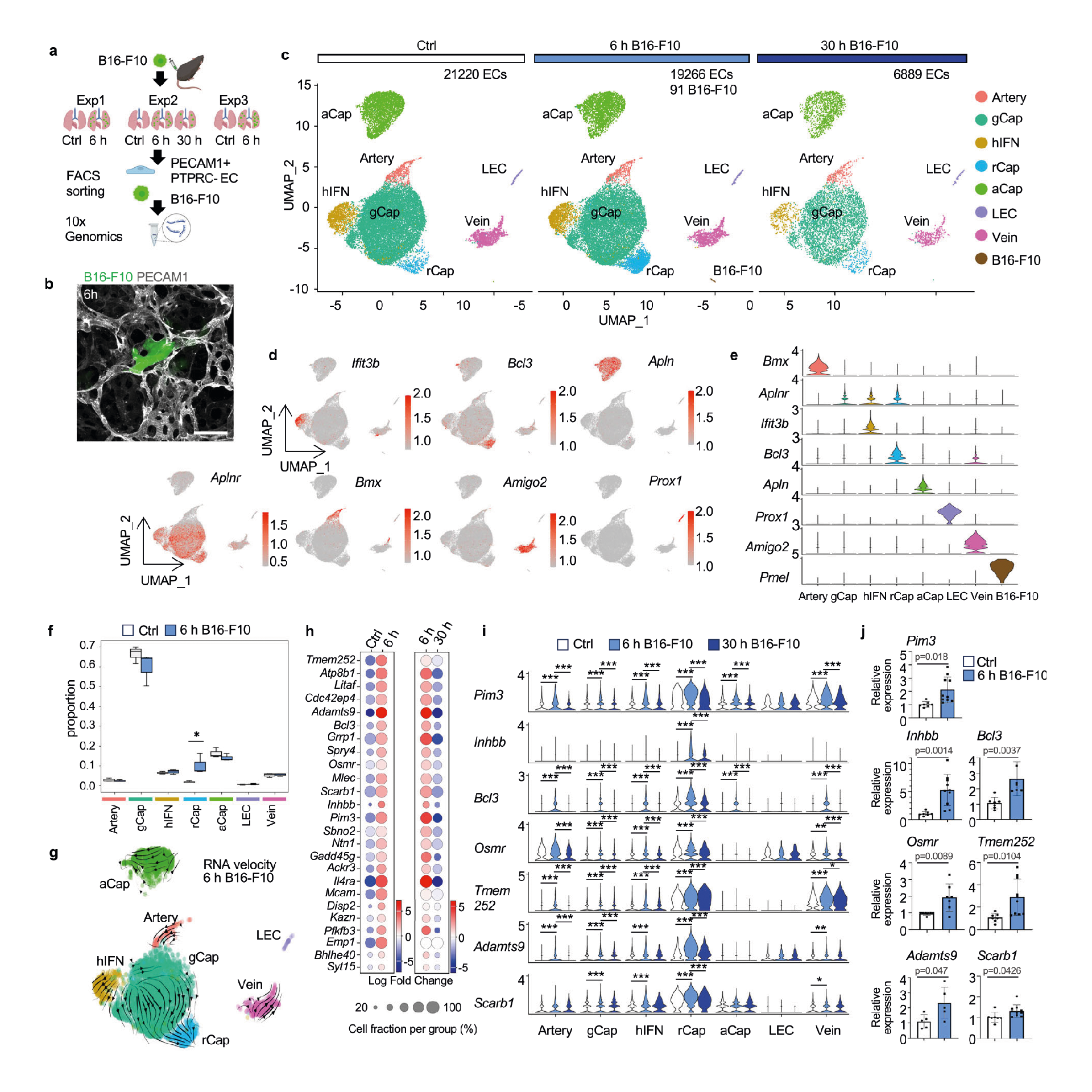
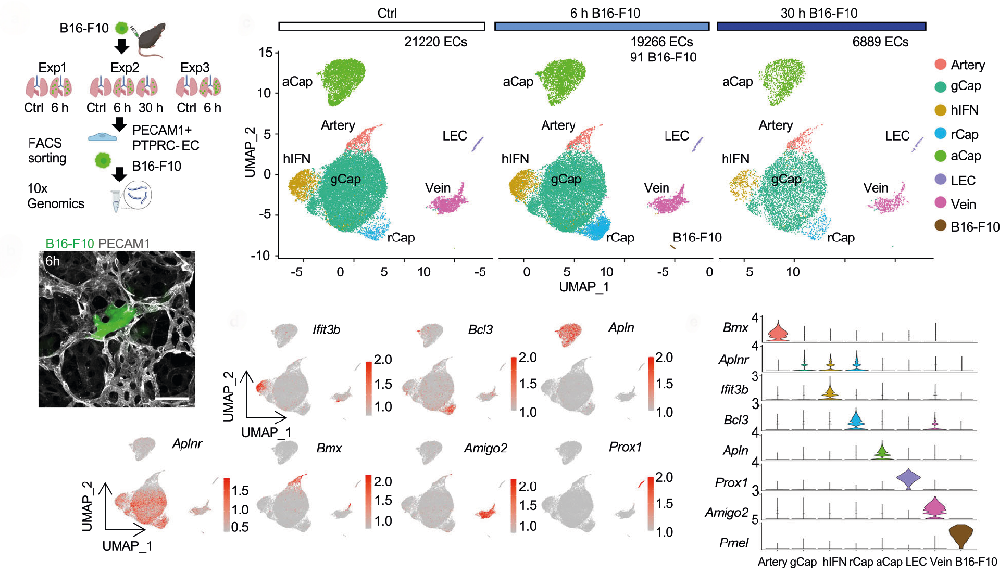
为了研究EC转录组在转移定植的第一步的变化,在黑色素瘤细胞注射后6小时从肺中分离Pecam1+ EC,并进行scRNASeq(图1a、b)。他们将gCap集群分成四个集群。其中包括表达相应标记基因的动脉和静脉毛细血管(CapA和CapV)(图1c-d)。此外,发现了一个额外的EC簇,除了gCap标记外,它还表达了独特的簇标记,并且在小鼠黑色素瘤注射后6小时细胞数量增加,因此,我们将其命名为反应性毛细血管EC (rCap)(图1c-f)。图1g的RNA速度分析表明rCap簇来源于gCap,与rCap表达的gCap标记一致。
RT-qPCR结果也证实,注射B16-F10 6小时后,小鼠肺上皮细胞中rCap顶端标记(包括Pim3、Bcl3、inhbb、Osmr、Tmem252、Adamts9和Scarb1)显著上调(图1j)。这些结果表明,循环黑色素瘤细胞诱导gCap的快速转录变化,导致肿瘤细胞到达肺部6小时后反应性毛细血管EC簇的扩增。
2.rCaps上调血管生成和炎症通路
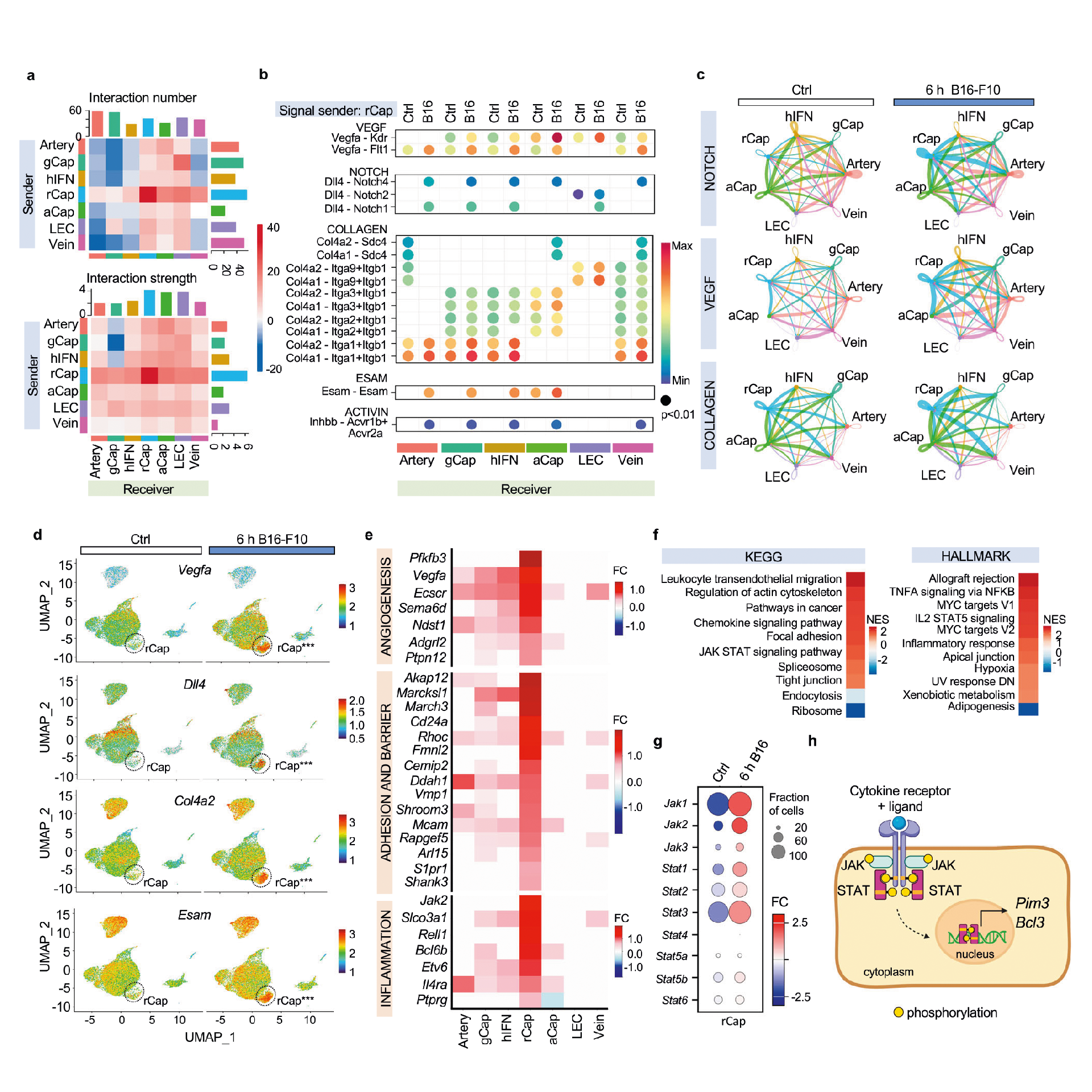
为了可视化转移性血管生态位中内皮细胞的旁分泌信号网络,接下来他们使用CellChat工具分析了细胞间通讯并在热图中表示(图2)。进一步分析发现crECs中Vegf、Notch、胶原、内皮细胞粘附蛋白ESAM和激活素通路上调(图2b-d),这些结果表明肿瘤细胞重新连接旁分泌EC信号通路,在转移性肺中富集rCap。
KEGG和GSEA分析也显示,转移肺和对照肺之间差异表达(DE) rCap基因的炎症、细胞骨架、粘附和紧密连接途径被激活(图2e, f)。
此外,rCap上调血管生成标志物,如糖酵解酶Pfkfb3、Jak2。此外,GSEA还发现rCap中JAK-STAT信号通路被激活(图2f, g)。我们知道JAK-STAT通路可以调节肿瘤血管生成和转移,而两个重要的rCap标记物Pim3和Bcl3是JAK-STAT通路的直接转录靶点(图2 h)。综上所述,这些结果表明rCaps在浸润黑色素瘤细胞时增加,其特征是血管生成标记物和JAK-STAT-PIM3-BCL3通路的转录上调。
3.rCap标记物定位于肿瘤细胞附近
为了定位肺内的rCap,他们使用RNAscope®原位杂交(ISH)检测rCap标记物Pim3、Bcl3和Inhbb(图3a-c),用抗黑色素瘤标志物PMEL抗体检测B16-F10细胞,用Pecam1探针检测ECs。有趣的是,Inhbb和Bcl3在对照肺中表达较低,但在转移肺中,Pim3、Inhbb和Bcl3均表达丰富,尤其是在黑色素瘤细胞附近(图3d-h)。分别有46%和16%的Pecam1+ ECs对Pim3和Bcl3或Pim3和Inhbb均呈阳性,表明在黑色素瘤注射后6小时,肿瘤诱导了rCaps的上调(图3i -l)。此外,与对照组相比,静脉注射B16-F10 7小时后肺溶物中PIM3蛋白水平升高(图3m, n)。综上所述,rCap标记物定位于浸润癌细胞附近的肺内皮。

4.rCap标记物在自发性转移过程中上调
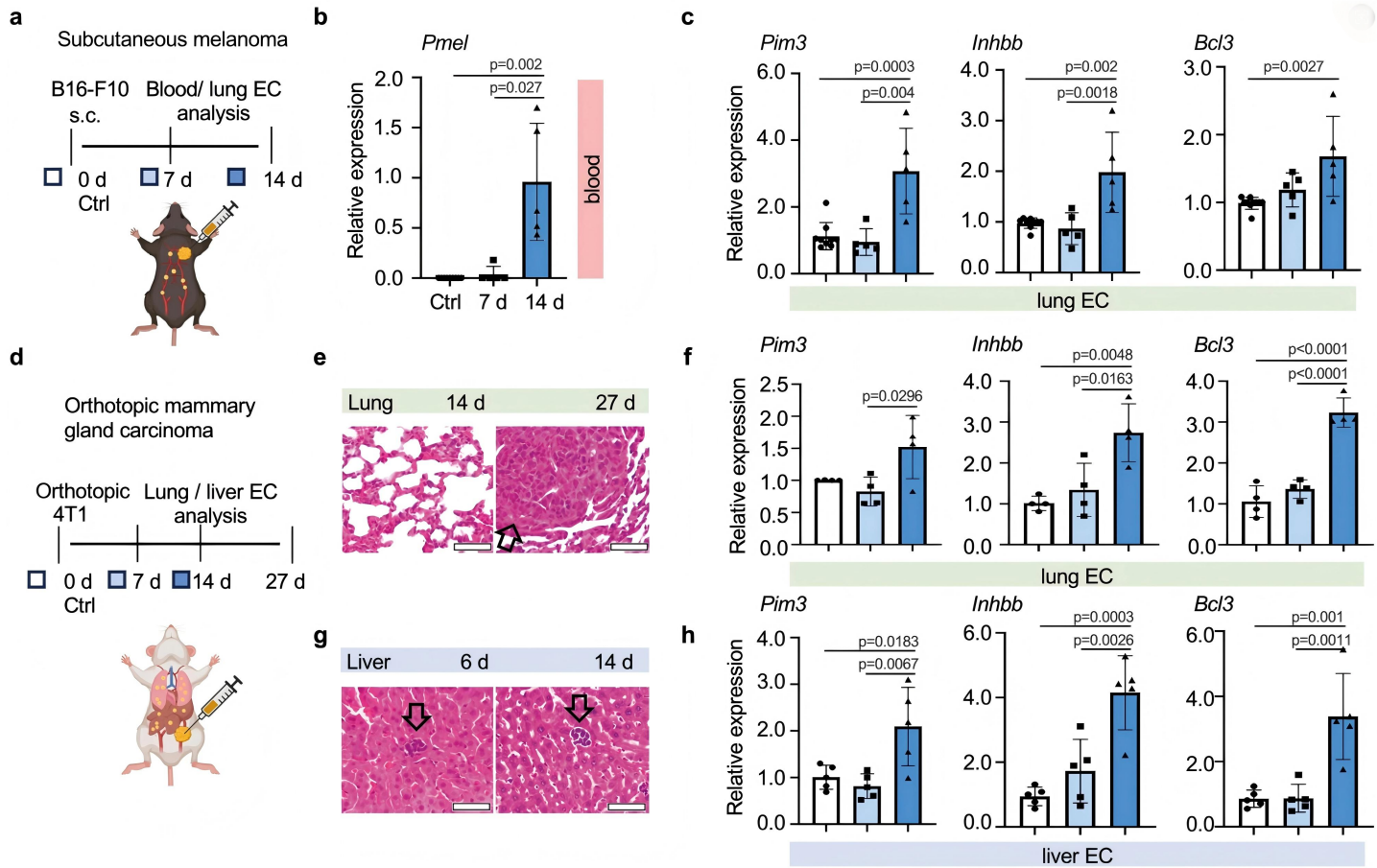
为了验证rCap在转移过程中的调节作用,他们使用了自发转移模型,这比静脉注射肿瘤细胞更能展现转移过程。为此,他们将B16-F10皮下接种到C57BL/6中,并在第14天形成了血管化肿瘤(图4a)。肿瘤细胞接种后第14天,血液样本中检测到CTCs(图4b),这在第7天时未曾出现。与此一致的是,在癌细胞接种后的第14天,Pim3、Bcl3和Inhbb在肺上皮细胞中上调,而在第7天则没有上调(图4c)。
接下来,他们使用原位4T1乳腺肿瘤模型,该模型在BALB/c小鼠中形成血管化肿瘤并转移到肺和肝脏(图4d-h)。这些结果表明,在自发转移过程中,肿瘤细胞在继发器官或循环中诱导rCap标记物的上调,而这种作用不是由原发肿瘤引起的。
5.肿瘤细胞分泌因子诱导rCap标记物
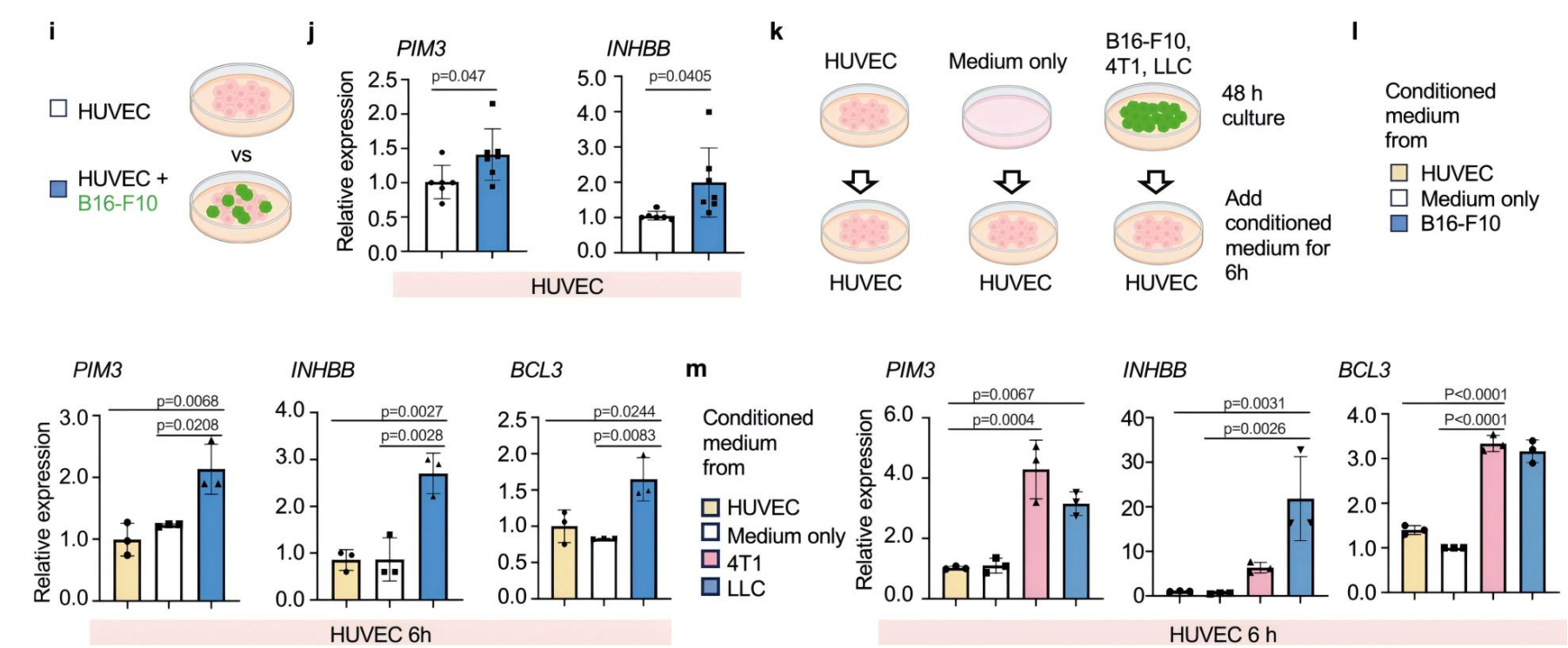
为了进一步研究肿瘤细胞诱导rCap标记上调的机制,他们将人脐静脉内皮细胞(HUVECs)与稳定表达绿色荧光蛋白(GFP)的B16-F10黑色素瘤细胞共培养和流式分选(图4f-g)。有趣的是,与单独培养的HUVEC相比,共培养后的HUVEC中PIM3和INHBB的表达增加,这表明肿瘤细胞足以诱导rCap标记物的上调(图4j)。此外,来自B16-F10、4T1或Lewis肺癌(LLC)培养的条件培养基同样诱导了PIM3、INHBB和BCL3的表达,这表明多种癌细胞类型的分泌因子诱导了培养的ECs中rCap标志物的表达(图4k-m)。因此,他们使用Bulk RNA-Seq方法比较了对照组和B16-F10条件培养基中培养16小时的HUVECs。文章的补充图中也展示了DE基因的GSEA分析结果,充分支持了黑色素瘤细胞分泌因子塑造肺毛细血管内皮的结论——导致特定的转录信号,以及JAK-STAT通路的激活。
6.rCaps与小鼠肿瘤血管系统的相似性
从前面的结果不难看出,与健康肺相比,转移性肺中rCap数量的增加以及rCap中血管生成标志物也上调,这促使研究者们开始探索rCap是否与肿瘤血管内皮相似。因此,他们分析了小鼠肺肿瘤EC Tax线上数据集,并发现尽管rCap标记物在肿瘤毛细血管中广泛表达,但rCap与PCV和缺口ECs的相似性最高。
7.rcap在人肺中形成明显的簇状结构
为了研究rCap是否也可以在人肺中发现,他们对小鼠肺EC数据集中的scRNASeq数据和人肺细胞图谱(HLCA)中的ECs进行了跨物种比较分析。通过分析来自健康肺和癌患者肺肿瘤邻近正常肺组织的EC亚群的scRNASeq数据,他们发现了一个额外的gCap簇,表达特定的标记物,包括ICAM1、EMP1、ARID5A和PIM3,并同样存在rCap基因特征的富集,表明它代表了人类rCap。
此外,在文章的补充图中他们也整合了人肺EC数据与他们的转移性小鼠肺EC数据,展示了rCap簇在小鼠和人类数据中共享约50%的rCap簇标记。
8.PIM3调节内皮屏障
接下来他们探究了PIM3的功能,通过使用PIM3 shRNA和选择性PIM抑制剂AZD-120815抑制HUVECs和BECs中的PIM激酶,发现与对照组(shScr)相比,沉默PIM3降低了EC表面粘附连接蛋白CDH5,并从内皮细胞-细胞连接处拆除钙粘蛋白-5和连环蛋白EC-EC连接的间隙,而CDH5的总水平不变,这表明PIM3特异性地维持了连接细胞表面定位的CDH5(图5a-e)。此外,与shScr ECs相比,连接CDH5与肌动蛋白细胞骨架的张力敏感α-catenin (CTNNA1)、β-catenin (CTNNB1)和δ-catenin (CTNND1)在shPIM3 ECs的细胞-细胞连接中也显著减少(图5f-m)。

AZD-1208处理的结果shPIM3沉默的结果一致(图6a, b)。这些结果表明,Pim3需要维持EC-EC连接的完整性,从而维持EC单层膜的屏障功能。
此外,为了研究PIM是否在体内也能调节连接复合体的完整性,他们对小鼠进行口服AZD-1208或载药5天,并对CDH5的厚肺切片进行染色(图6h -l)。对照小鼠肺泡毛细血管中EC-EC连接之间的CDH5染色是连续的,而AZD-1208处理小鼠的肺中观察到CDH5连接的间隙(图6h -l),这表明,与体外实验结果一致,PIM抑制降低了小鼠肺中EC-EC连接中的CDH5。

9.Pim抑制增加肺血管渗漏和转移
为了研究Pim介导的EC连接完整性调节在体内的功能意义,他们通过给小鼠口服Pim抑制剂AZD-1208三天,并通过注射70 kd荧光葡聚糖10分钟静脉注射来分析血管渗漏。结果发现AZD-1208处理的肺中有强葡聚糖信号,表明示踪剂渗漏,而对照组肺显示低信号,表明AZD-1208损害了肺中的EC屏障功能。
由于已知肺血管屏障对转移性肿瘤细胞形成障碍,他们接下来便对AZD-1208影响转移性黑色素瘤在肺部的定植进行了研究。首先静脉注射B16-F10黑色素瘤细胞,让其在肺部定植3天,然后每天给药AZD-1208治疗5天(图7a-d),发现AZD-1208增加了肺转移结节和渗漏的数量。这些结果表明,PIM抑制增加血管渗漏和转移性定植,但不影响转移结节形成后黑色素瘤的生长。
此外,他们在4T1和LLC注射前4-5天给小鼠注射AZD-1208,并在肿瘤细胞注射后7天和14天分别监测转移情况。发现AZD-1208增加了两种模型中转移结节的数量(图7e-j)。因此,他们的研究结果表明,癌症反应性EC标记物PIM3在癌细胞定形过程中保护EC屏障。而PIM抑制增加了不同癌症类型的血管渗漏和肺定植。

以上结果表明,通过结合scRNASeq、Bulk RNASeq和小鼠肺同系性肺泡间质转移模型,他们揭示了小鼠和人类肺部的反应性毛细血管EC特性,展现了肺内皮对肿瘤细胞的可塑性,证明了PIM3的屏障保护作用和PIM抑制剂对血管通透性的影响,可能部分解释了PIM抑制剂在癌症试验中疗效有限的原因,为后续的改善治疗提供新思路。
 技术咨询:
技术咨询: