免疫细胞“大军”如何影响肿瘤微环境?一篇读懂免疫细胞浸润分析
2026-03-06
Q “肿瘤微环境”&免疫细胞浸润?
当我们谈论肿瘤治疗时,常常会听到 “肿瘤微环境” 这个专业术语。而在肿瘤微环境这个复杂的网络中,免疫细胞扮演着至关重要的角色。免疫细胞浸润 构成肿瘤微环境(TME)的关键组分,其组成异质性直接影响疾病进展与转归。
接下来就让我们一起揭开免疫细胞浸润分析的神秘面纱。
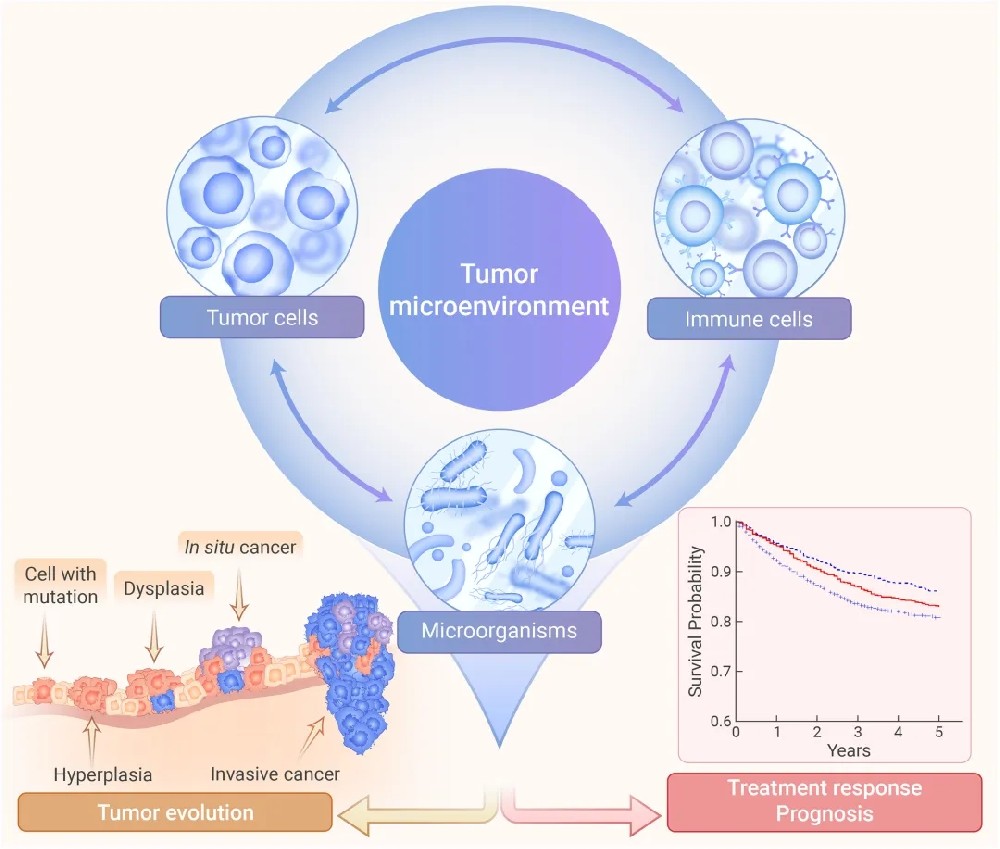
图1.肿瘤微环境会影响肿瘤的发展,并影响对癌症治疗的反应 Q “什么是免疫细胞浸润? 免疫细胞浸润指的是免疫系统的细胞(如T细胞、B细胞、巨噬细胞、NK细胞等)迁移到特定的组织或器官,并发挥相应的免疫作用。这一过程在生理和病理条件下均可发生,例如正常免疫监视、炎症反应、肿瘤微环境调节、移植排斥等。 想象一下,肿瘤区域就像一个被敌军占领的城堡。免疫细胞就是我们身体派出的“特种部队”,离开血液渗透到肿瘤组织内部,识别并消灭癌细胞。 图2.通过空间多组学所揭示的“肿瘤免疫微环境”图景 Q “为什么免疫细胞浸润分析如此重要? 预测治疗反应 高水平的免疫细胞浸润通常意味着患者对免疫治疗可能有更好的反应。 评估预后 某些免疫细胞的存在与患者生存期延长密切相关。 理解耐药机制 分析为什么有些肿瘤能够“逃逸”免疫系统的攻击。 开发新疗法 为个性化免疫治疗提供科学依据,帮助科学家发现新的治疗靶点,例如针对特定抑制性细胞的药物。 图3. 免疫细胞浸润技术路线 组织病理学方法 (1)免疫组化(IHC):传统金标准,可视化特定免疫细胞。 (2)流式细胞术:定量分析细胞表面标志物。 (3)多重免疫荧光:同时检测多种免疫细胞类型。 (4)原位杂交:验证特定基因在特定细胞中的表达。 计算生物学方法 用计算生物学方法进行免疫细胞浸润分析,核心思想是:不直接“看”细胞,而是通过对肿瘤组织的基因表达数据进行数学“反卷积”,来推断其中各种免疫细胞的比例和状态。这是一个从“混合信号”中拆解出“组分信息”的过程。 图4.计算生物学方法的主要技术路线 (1)基于基因表达的反卷积(如CIBERSORT, xCell) 原理: 将肿瘤组织的整体基因表达谱,视为各种细胞(免疫细胞、癌细胞、基质细胞等)表达信号的线性混合。算法通过一个已知的“特征基因矩阵”,解构混合信号,估算出各类细胞的相对比例 典型流程: 1.输入:肿瘤样本的批量RNA-seq或芯片数据。 2.算法核心: ①CIBERSORT:使用线性支持向量回归,匹配22种免疫细胞的特征表达谱,输出比例分数(总和为1)。 ②xCell:基于基因集富集分析思路,计算64种免疫和基质细胞的富集分数,反映其活性/丰度。 3.输出与解读:得到一个“样本×细胞类型”的矩阵。 4.后续分析: 差异分析:比较不同组别(如癌 vs. 正常,疗效好 vs. 差)的细胞浸润差异。 生存分析:将细胞比例与患者生存期关联,找出预后相关的细胞类型。 相关性网络:分析不同免疫细胞间的共现或互斥关系。 (2)单细胞RNA测序 原理: 将肿瘤组织的整体基因表达谱,视为各种细胞(免疫细胞、癌细胞、基质细胞等)表达信号的线性混合。算法通过一个已知的“特征基因矩阵”,解构混合信号,估算出各类细胞的相对比例。 典型流程: 实验与数据生成: 组织解离 → 单细胞捕获与建库 → 高通量测序。 2.生物信息学分析: ①质控与过滤:去除低质量细胞和死细胞。 ②标准化与降维:使用PCA、t-SNE或UMAP等技术将高维数据降至2D/3D可视化。 ③细胞聚类与注释:根据基因表达相似性将细胞聚类,并利用已知标志基因(如CD3E、CD8A代表CD8⁺T细胞)为每个细胞簇赋予生物学身份。 ④轨迹与通讯分析:推断细胞分化轨迹(如T细胞耗竭过程),分析细胞间配体-受体相互作用。 3.输出与解读: 可精确量化各类免疫细胞亚群的比例,并深入分析其功能状态(如耗竭、激活、增殖)、克隆扩增(通过TCR/BCR测序)和潜在调控网络。 (3)空间转录组学 原理: 在保留组织切片空间结构的同时,测量切片上每个特定位置(“斑点”)内所有细胞的转录组信息。一个斑点可能包含数个细胞。 典型技术: 1.基于芯片捕获:如10x Visium,将组织切片覆盖在带有空间条形码的芯片上,进行高通量测序。分辨率约55微米(覆盖数个细胞)。 2.基于成像:如MERFISH, seqFISH,通过多重荧光原位杂交成像,可达到亚细胞级分辨率,但通量较低。 典型分析: ①空间基因表达可视化:将特定基因(如CD8A)的表达映射回组织原位上直接看到“杀手T细胞”富集在肿瘤边缘还是核心。 ②与scRNA-seq数据整合:这是关键分析策略。将高分辨率的scRNA-seq数据作为“细胞图谱参考”,去解卷积空间转录组每个斑点的混合信号,从而推断出每个斑点内可能的细胞类型组成及其空间分布。 ③空间邻域与微环境分析:定义“肿瘤-免疫边界区”、“三级淋巴结构”等功能区域,并分析不同区域特有的细胞群落和基因表达程序。 研究背景 为改善结直肠癌,特别是免疫治疗不敏感型患者的预后,寻找新的生物标志物和潜在治疗靶点。 核心分析步骤 第一步:宏观画像——量化免疫浸润全景。
(1)数据来源:从TCGA(癌症基因组图谱)和GEO(基因表达汇编) 数据库中,获取了大量结直肠癌患者的批量RNA-seq转录组数据。
图5. GEO 和 TCGA 数据库中癌症组织与正常组织之间免疫细胞评分的差异。
(2)核心算法:使用 ssGSEA 算法进行“反卷积”分析。简单说,就是依据28种已知免疫细胞的独特基因表达特征,像“听音辨人”一样,从肿瘤组织的混合基因表达信号中,推算出每种免疫细胞的相对浸润丰度。这一步得到了每个样本的“免疫细胞浸润图谱”。
第二步:聚焦核心——锁定关键免疫细胞 (1)分析方法:面对28种细胞的复杂图谱,研究者采用LASSO回归和支持向量机递归特征消除这两种机器学习算法,对浸润分数进行降维和筛选。 (2)关键发现:最终锁定7种对结直肠癌微环境最具影响力的核心免疫细胞,包括:活化B细胞、效应记忆CD4 T细胞、未成熟B细胞、肥大细胞、单核细胞、自然杀伤T细胞、1型辅助T细胞 (Th1 cells)。 微观验证——单细胞层面上的终极确认与新发现 (1)数据跃迁:为了验证上述发现并寻找具体靶点,研究切换到了分辨率更高的 单细胞RNA-seq数据。 (2)具体操作:在GSE225857这个单细胞数据集中,研究者成功地在单个细胞水平上,识别并确认了上述关键免疫细胞亚群的存在。 (3)核心基因发现:通过差异表达分析,他们发现了一个名为RGS1的基因,在多个关键的免疫细胞亚型(如效应T细胞、耗竭T细胞、巨噬细胞)中显著高表达。 (4)RGS1的功能解读:RGS1是一个调节G蛋白信号的基因,参与调控细胞迁移和激活。在肿瘤微环境中,它可能扮演一个“复杂的调控开关”角色:一方面,它可能促进某些免疫细胞向肿瘤部位迁移;另一方面,它也可能参与抑制免疫细胞过度活化。这个基因的发现,为理解免疫微环境的调控机制提供了一个新的切入点。 图6. 关键免疫微环境基因的选择及与单细胞转录组学的差异分析。 随着单细胞技术和人工智能的发展,免疫细胞浸润分析正朝着更高精度、更全面的方向发展: 1.动态监测:治疗过程中实时跟踪免疫细胞变化 2.空间分析:不仅知道“有什么细胞”,还知道“细胞在哪里” 3.多组学整合:结合基因组、蛋白组数据,全面解析肿瘤-免疫相互作用
免疫细胞浸润分析如同一扇窗口,让我们得以窥见肿瘤微环境中免疫系统与癌细胞之间的复杂博弈。随着分析技术的不断进步,我们有理由相信,更加精准的免疫治疗时代正在到来。免疫系统是我们身体自带的抗癌武器,而免疫细胞浸润分析,正是我们理解并增强这一武器的关键地图。
Ugai T, Yao Q, Ugai S, Ogino S. Advancing precision oncology: Insights into the tumor microenvironment and immunotherapy outcomes. Innovation (Camb). 2024 Jun 7;5(4):100656. doi: 10.1016/j.xinn.2024.100656. PMID: 39021526; PMCID: PMC11253650. Hsieh WC, Budiarto BR, Wang YF, Lin CY, Gwo MC, So DK, Tzeng YS, Chen SY. Spatial multi-omics analyses of the tumor immune microenvironment. J Biomed Sci. 2022 Nov 14;29(1):96. doi: 10.1186/s12929-022-00879-y. PMID: 36376874; PMCID: PMC9661775. Yang Liu and Teng Chen. 2024. Identification of Key Genes in the Colorectal Cancer Immune Microenvironment Through Integrated Analysis of Immune Infiltration Algorithms and Single-Cell Transcriptomics. In Proceedings of the 2024 4th International Conference on Bioinformatics and Intelligent Computing (BIC '24). Association for Computing Machinery, New York, NY, USA, 408–413. https://doi.org/10.1145/3665689.3665757. END
 技术咨询:
技术咨询: