TCR-seq揭示高危肺部毛玻璃样混浊病变的PD-1免疫治疗效果
2024-06-24
本期介绍的这篇文章发表在Signal Transduction and Targeted Therapy (2024) 9:93 ; https://doi.org/10.1038/s41392-024-01799-z。研究者设计并进行了一项单组II期临床试验(NCT04026841),通过TCR-seq等研究方式,探索PD-1阻断治疗早期疾病期间的免疫动力学改变。
前言:肺癌是世界上第二大最常诊断的癌症,其中约85%是非小细胞肺癌(NSCLC)。目前研究表明针对程序性细胞死亡(PD-1)和程序性死亡-配体 (PD-L1)轴的免疫检查点抑制剂(ICIs)可显著延长晚期NSCLC患者的总生存期(OS)。
然而,免疫治疗对超早期非小细胞肺癌微创甚至侵袭前病变的效果尚不清楚。临床上根据肺癌CT筛查可分为纯毛玻璃样肺结节(GGO)和部分固体状肺结节,不同放射学类型的肺癌在生物学行为上存在显著差异。与表现为实性结节的肺癌相比,与GGO相关的肺癌的临床进程较为缓慢,其特点是代谢不活跃,免疫微环境不活跃。
多发性原发性肺癌(Multiple primary lung cancer, MPLC)在CT上多表现为多发GGO,常规选择是切除主要病变,然后密切监测剩余病变。但是,对于患者术后未切除且进展风险高的病变的处理,往往是临床一大难题。此前有研究表明,在肺癌的侵袭前阶段存在免疫逃逸,因此,研究PD-1抑制剂在高风险肺GGO病变中的应用是非常有意义的。
我们知道,T细胞反应对癌症患者的抗肿瘤免疫至关重要,循环和肿瘤浸润T细胞的状态与患者对免疫治疗的反应息息相关,此外,既往研究表明,t细胞受体(TCR)的特征(克隆性和多样性)可能是免疫检查点抑制剂(ICIs)治疗NSCLC患者的潜在生物标志物。
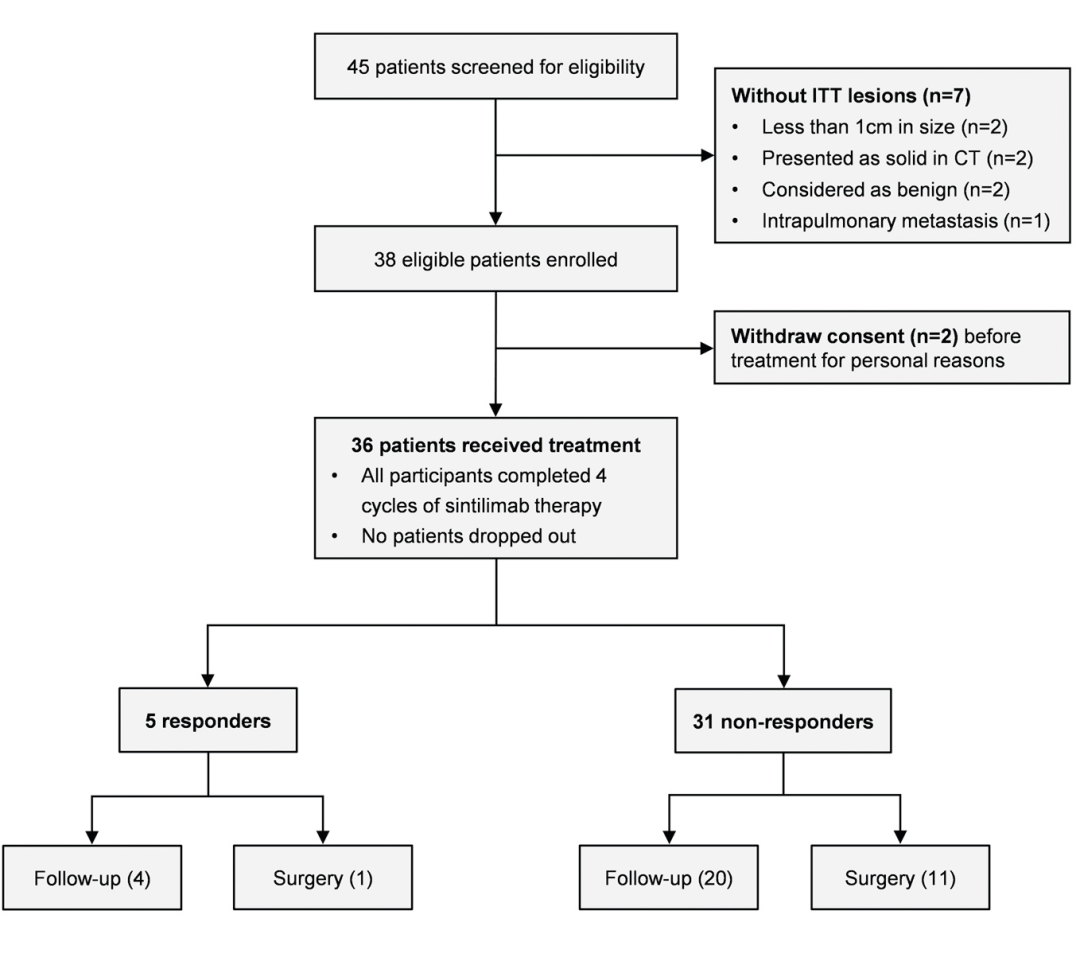
图1是筛选符合纳入条件的患者流程图
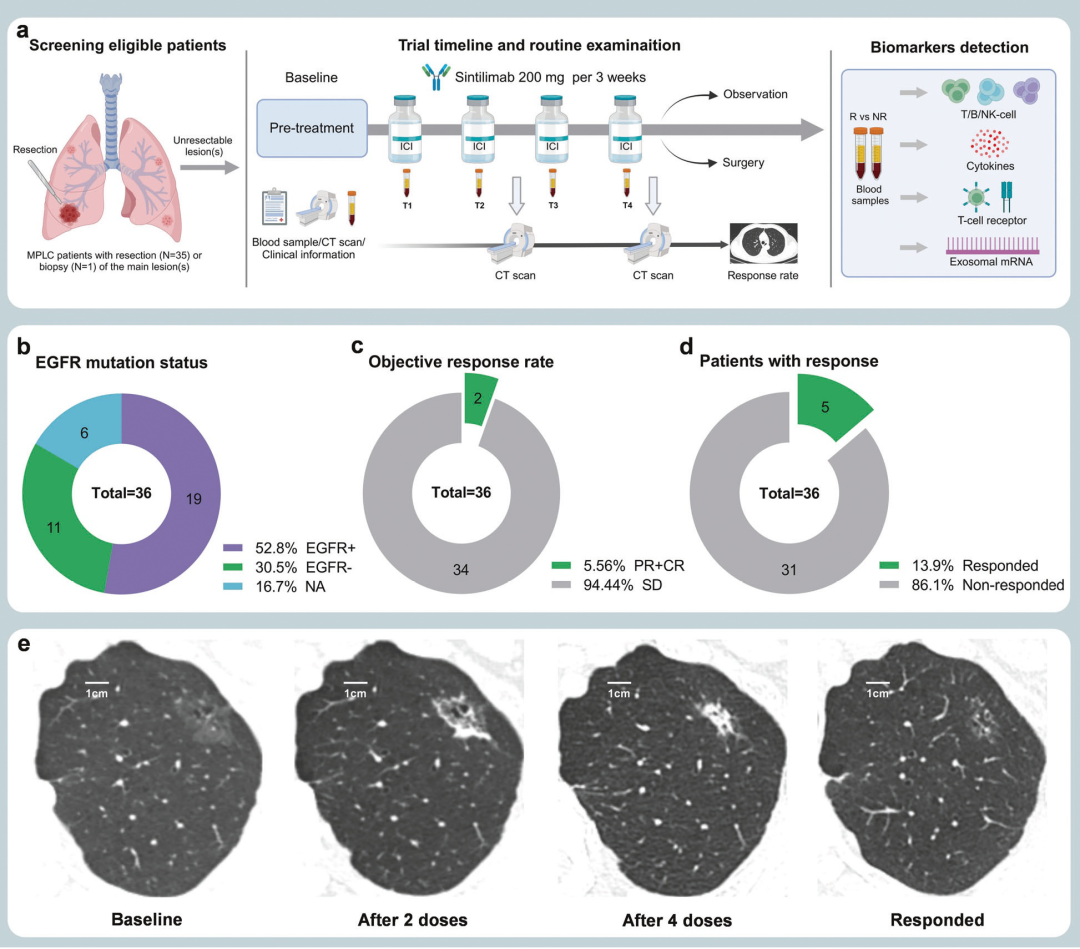
图2是试验时间、检查和研究的结果展示
其中的生物标志物包括T/B/ nk细胞亚群、T细胞受体(TCR)、细胞因子和外泌体RNA,在反应者和无反应者之间进行监测和比较。图2b是患者主要病变的切除组织或活组织的EGFR突变情况。图2e 展示了1例经sintilimab单抗治疗后取得显著疗效的患者胸部CT放射学改变。
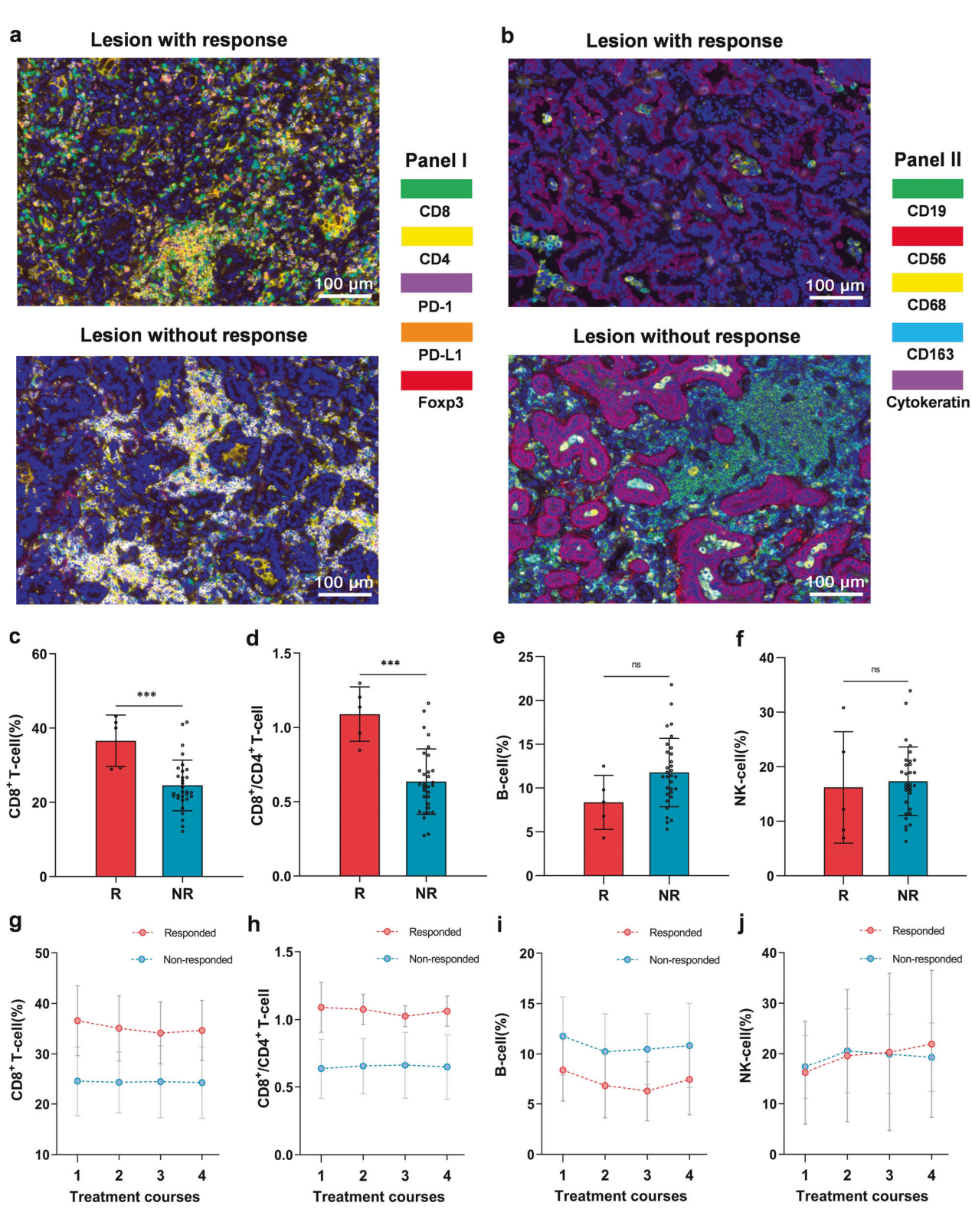
图3
当全部用药完成后,研究者对9例患者的肿瘤标本进行基因检测,均为EGFR突变阳性。随后进行mIHC分析,通过染色发现mIHC中各种免疫细胞的详细结构和比例(图3a, b)。
期间,研究者对有反应者和无反应者在用药周期内各种免疫细胞比例的变化趋势加以监测(图3 c-j)。
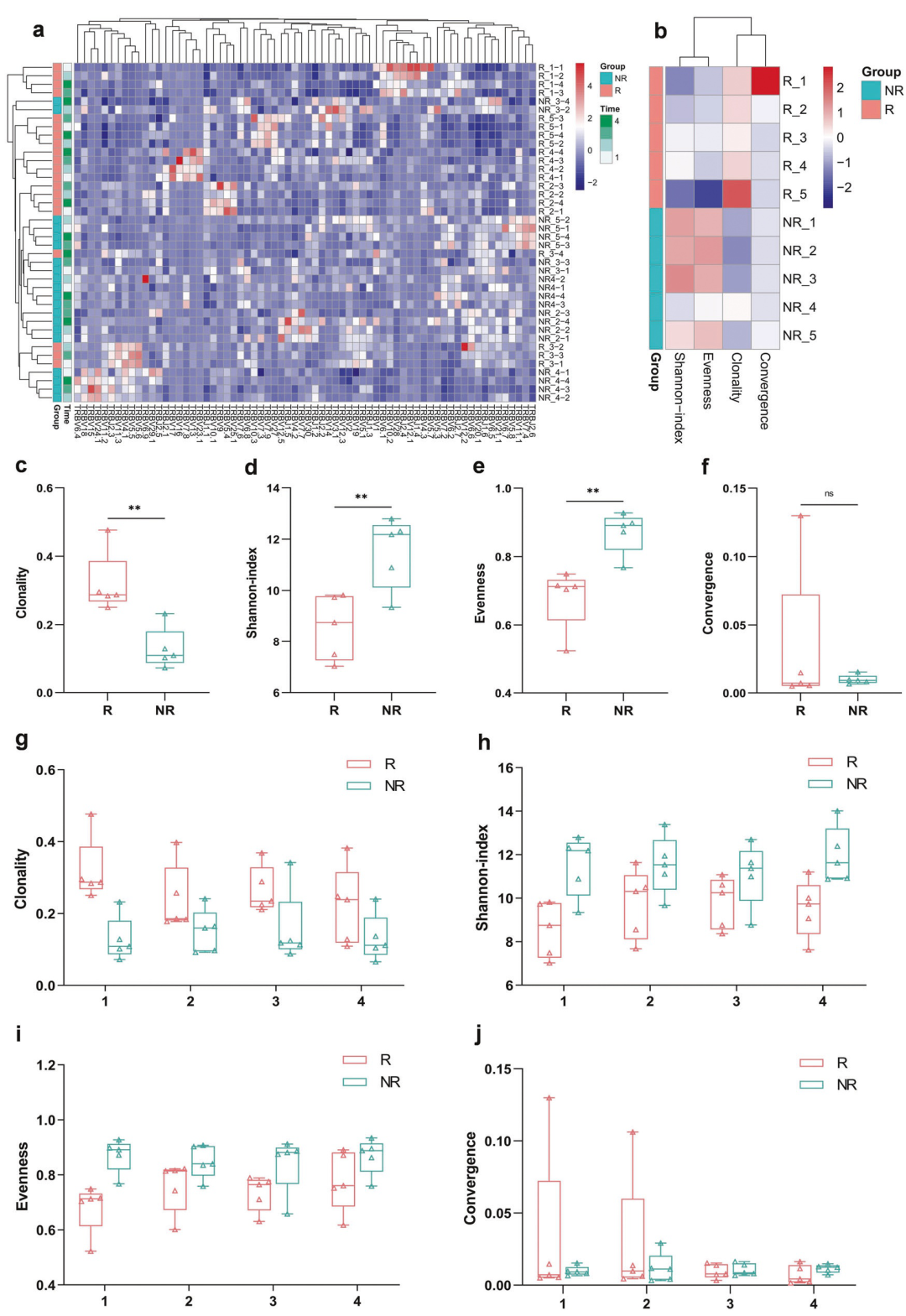
图4
随后,研究者对5例应答患者(r组)和5例相似临床特征的无应答患者(nr组)血液样本进行TCR-seq、细胞因子和外泌体RNA检测(图4)。
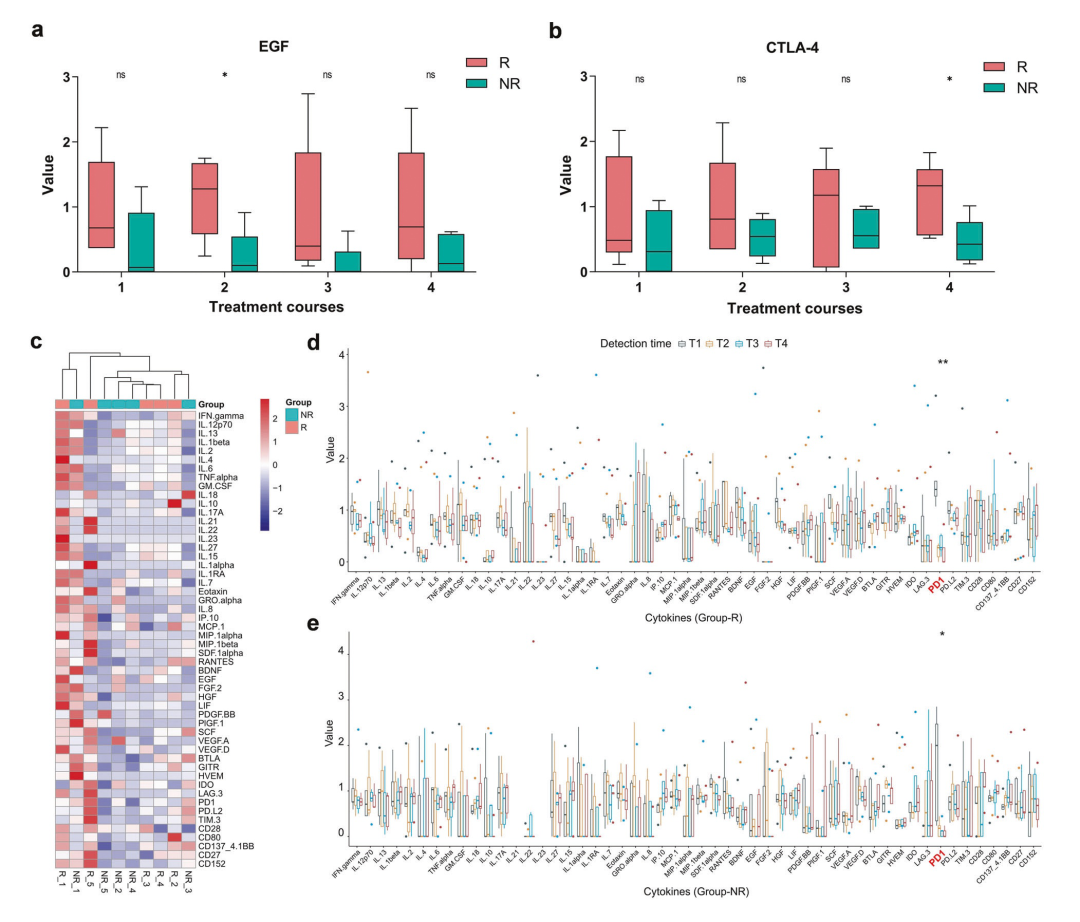
图5
图5是对r组(n = 5)和nr组(n = 5)患者细胞因子检测结果展示。包括45个细胞因子和14个免疫检查点,其中r组(红色)和nr组(绿色)患者各时间点(T1-T4) EGF (图5a)和CTLA-4 (图5b)的浓度均存在差异性。并根据治疗前血液中细胞因子对两组患者进行聚类分析(T1)。

图6
接着,研究者们对获得的患者外泌体RNA进行分析,联合TIDE计算方法,最终10例患者中有9例预测正确(r组4例,nr组5例)(图6a)。然后根据MsigDB的50个“Hallmark”,进行GSEA富集分析,比较r组和-NR患者之间的基因表达谱(图6b) 。
分析发现对于r组(vs. -NR)患者,上调的基因标志是Myc targets_v2,下调的基因标志包括脂肪酸代谢、氧化磷酸化(OXPHOS)和蛋白质分泌。另外研究者还分别对两组给药后的上调和下调基因(T2/T3/T4 vs. T1)进行评估。如图6c所示,在有应答和无应答患者中,分别有1220和1032个基因上调,367和215个基因下调;并只存在少量重叠(分别为149个[7.1%]和6个[1.0%])。
采用时间序列将表达趋势相似的基因进行聚类分析,在r组和nr组中分别鉴定出10个簇(时间序列基因表达趋势),其中,r组中的4个簇和nr组中的2个簇在给药后表现出显著的基因表达上调或下调(图6d, e)。值得注意的是,在r组中,簇1和6所代表的趋势具有特异性,另外2个簇(簇8和10)与nr组具有相同的趋势。KEGG和GO富集分析,揭示了由两个特定簇代表的这些基因和途径(图6f, g)。在r组中,簇1主要表达了氧化磷酸化和非酒精性脂肪性肝病途径的下调,以及与NADH脱氢酶活性和氧化还原酶活性相关的基因表达下调;簇6显示泛素偶联酶活性的相关基因表达上调。
 技术咨询:
技术咨询: